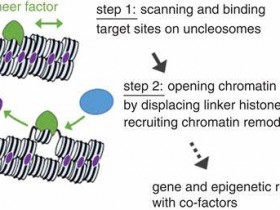
研究DNA -蛋白相互作用是分子生物学的一个重要方面,其研究方法多种多样,如染色质免疫沉淀(ChIP)检测、电泳迁移率变动分析(EMSA)、荧光素酶报告法、膜过滤结合分析法、酵母单杂交系统等。另一个有助于研究DNA -蛋白质相互作用的有趣实验是DNA足迹分析,1978年由Galas和Schmitz建立,它是早期用于研究这些相互作用的技术之一,是对Maxam-Gilbert测序技术的修改。
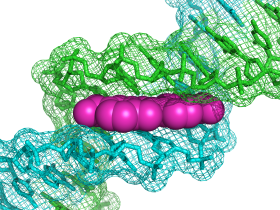
这种技术的基础是,DNA结合蛋白保护DNA,使其不受已知的裂解或修饰DNA的外部分子的作用。简而言之,正在研究的一种蛋白质被添加到含有假定蛋白质结合位点的DNA片段中,用裂解剂或改性剂处理DNA,并在聚丙烯酰胺凝胶上运行。与没有添加蛋白质的对照DNA相比,测试DNA将会显示出目的蛋白与DNA结合的缺口或“脚印”,这个区域可以被分析并确定为一个潜在的蛋白质结合位点。
具体步骤如下:
- PCR扩增并标记感兴趣的区域,一个预测的蛋白结合位点。
- 在被标记的扩增DNA中加研究的入蛋白质,做一个只有DNA没有蛋白质的对照管。
- 免疫沉淀蛋白结合DNA。
- 添加一个修饰或裂解剂。
- 用聚丙烯酰胺凝胶电泳(PAGE)运行这两个样品
- 对照样本将形成一个统一的条带,而测试样本将显示在蛋白质保护DNA模式中的缺口(如果结合)。
- 做一个比较分析来确定蛋白质被限制的确切序列。

做这个实验需要什么?
一、DNA
1.用一个100到400个bp的片段进行实验
2.PCR可以从质粒或基因组DNA源扩增DNA,或直接从质粒中消化DNA片段。
二、标记DNA
- 标记DNA以识别片段并进行分析。传统来说,使用32P末端标记,凝胶通过放射自显影法呈现。放射性标记对于少量的DNA是非常敏感和最理想的,但是放射性工作的危害已经导致了替代技术的使用。荧光标记更安全,但对低浓度的DNA不够敏感。
- 如果DNA通过PCR扩增,则直接在PCR反应中使用标记的引物进行末端标记。
- 如果DNA是从克隆的质粒中消化来的,用酶促的方式将标签添加到DNA上,然后用一个聚合酶把它们填入标记的核苷酸中。
- 纯化标记的DNA,用柱或乙醇沉淀去除未标记的探针。
三、蛋白质
- 使用用纯化的蛋白质代替粗制的裂解物。
- 允许DNA -蛋白质在适当的缓冲液和在优化的条件下结合。
- 使用对蛋白质和protein A/G特异性抗体对复合物免疫沉淀,将DNA -蛋白质复合物从未结合的分子中分离出来。
四、选择断裂剂或改性剂
- 一个好的试剂不应该是特异性序列(在DNA的随机位点进行切割或修改),而且应该易于使用和控制。
- DNaseI是一个传统的选择,因为它是一个双链的核酸内切酶。它的大尺寸容易造成物理障碍,并且通过添加EDTA很容易控制。另一方面,由于它的活动受到局部DNA结构的影响,它不会随机地进行切割,从而导致了一个不均匀的梯状。另外,DNase I是一个大的分子,由于空间位阻,它不能与临近的DNA结合蛋白结合。
- 由芬顿反应(Fe2+被H2O2还原)产生的羟基自由基用于引起DNA断裂。它们是序列中性的,它们的小尺寸提供更高的分辨率。但是缓慢的消化反应使过程耗时。
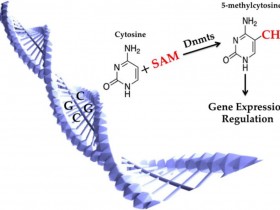
- 硫酸二甲酯(DMS)混入甲基嘌呤在DNA链上,甲基化DNA在添加蛋白质之前,蛋白质结合在甲基化位点被阻止。在处理和去除感兴趣的蛋白质后,用哌啶或氢氧化钠处理,在修改后的碱基上切割。
- 紫外线辐射也被用来造成DNA断裂,紫外线反应迅速,有助于捕捉短暂的蛋白质结合,并能在体内使用,因为它能很容易穿透细胞膜。但是这种分析的凝胶很难解释。
五、反应条件
- 在足迹分析前,用源DNA优化改性条件和试剂浓度。
- 调整反应条件,使每个DNA分子有一个切割或修饰。在开始试验之前,测试一系列的浓度,包括修饰剂和DNA比值,以及对照DNA样品的反应时间,以确定最佳条件。
六、PAGE
- 使用一种变性聚丙烯酰胺凝胶来分离断裂的片段。
- 每个孔上样等量的蛋白以进行比较。
- 在凝胶运行完成后,使用放射自显影或荧光显影曝光。
- 通过与对照相比较,确定测试样品中缺失的条带。
- 可以使用自动分析软件来帮助解释足迹凝胶。
尽管DNA足迹分析可能看起来古老而复杂,并且被新的替代方法和改良物所取代,如ChIP-seq, x射线晶体学等,它仍然是研究DNA-蛋白质相互作用的一种重要的方法。