细胞死亡的类型不再只是细胞凋亡和细胞坏死,细胞的另一种死亡方式还有细胞焦亡。那细胞焦亡的机制是什么?那么赶快来看pyroptosis——细胞焦亡。
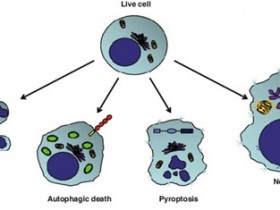
说起细胞凋亡大家都很熟悉,那细胞焦亡呢?可能很多人的第一反应是:什么鬼?细胞凋亡他弟?其实细胞焦亡本质上是一种程序性细胞坏死,与细胞凋亡有许多不同。下面让我们一起来好好了解下他。
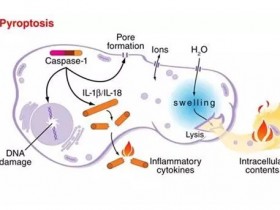
细胞焦亡(pyroptosis)是一种最近发现的细胞程序性死亡方式,表现为细胞不断胀大直至细胞膜破裂,导致细胞内容物的释放进而激活强烈的炎症反应。细胞焦亡是机体重要天然免疫反应,在拮抗感染和内源危险信号中发挥重要作用。相比于细胞凋亡(apoptosis),细胞焦亡发生的更快,并会伴随大量促炎症因子的释放。
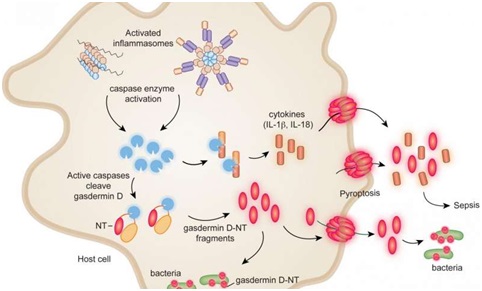
来自北京生命科学研究所(NIBS)、同时也是药明康德生命化学研究奖得主的邵峰院士首次揭示和阐明了细胞焦亡的机制。邵峰院士团队在体外实验通过沙门氏菌(一种胞内菌)感染细胞,免疫荧光显微镜观察到细胞发生程序性死亡,早期认为这种形式的死亡为凋亡,其实它是另一种死亡方式,细胞焦亡。重要的一点是,这个培养基中需要加入 IL-1β。因此他们将研究方向集中在胞内菌介导 IL-1β产生相关的炎症通路上,进而发现了感受胞内菌的重要识别受体。他的团队发现,半胱天冬酶(caspase)炎症小体下游的Gasdermin家族蛋白可能在细胞焦亡中发挥了关键作用。现已知,caspase-1/4/5/11通过切割由500多个氨基酸组成的Gasdermin家族蛋白之一GSDMD,使后者N、C两端的结构域分开,进而释放N端的片段。GSDMD蛋白N端片段可以识别并结合细胞膜上的磷脂类分子,并进一步在细胞膜形成孔洞,导致细胞渗透压变化,最终使得细胞膜裂解,发生焦亡。长期以来 IL-1β如何释放至细胞外始终不得而知,该团队推测可能 Gsdmd 是 IL-1β释放至细胞外的必要条件。他们发现敲除 Gsdmd 不影响 IL-1β的产生,但明显影响分泌。由此可见 IL-1β在细胞焦亡中扮演重要角色,武汉艾美捷科技有限公司的新品人IL-1βELISA检测试剂盒隆重上市,助力科研,敬请期待!
按照功能 capases 可以分为两大类,分别参与细胞凋亡和细胞焦亡。凋亡相关的包括 CASP2,CASP8,CASP10,CASP3,CASP6,CASP7,以及 CASP9。CASP1,CASP11,CASP4 和 CASP5 是炎症相关的 capases,参与细胞焦亡(pyroptosis)。Caspase1 的激活主要发生在巨噬细胞或树突状细胞中,可诱发细胞焦亡。细胞焦亡也是 Caspase 4/5/11 激活后的主要应答反应,在巨噬细胞和非巨噬细胞中均可发生。
细胞焦亡如何发生的呢? gasdermin 家族的 N 端结构域在细菌中也显示出明显的致死毒性。这一现象暗示 gasdermin N 端结构域可能是通过直接破坏细胞膜而产生杀死细胞。为了验证这一假设,邵峰院士团队通过生物化学和荧光显微成像的细胞实验,进一步证实,在真核细胞焦亡过程中,活化的 gasdermin N 端结构域会从细胞质中转移到细胞膜上,细胞随后出现体积膨胀和焦亡的现象。此外,活化的 gasdermin N 端结构域重组蛋白只能从真核细胞内部破坏细胞膜。利用脂质体泄漏实验,该团队进一步发现 gasdermin N 端结构域能够高效特异地破坏含有 4, 5- 二磷酸磷脂酰肌醇或心磷脂的脂质体,在脂膜上聚合形成规则的孔道。利用负染电镜的方法,他们首次观察到 gasdermin N 端结构域能在特异磷脂或天然磷脂组成的膜上打孔,形成很多蜂窝状的孔道,这些孔道的内径约 10-14nm。进一步的电镜分析揭示这些分子孔道具有 16 重对称性,表明 gasdermin N 端结构域在膜上形成 16 元聚合体的孔道。该孔道的内径大约为 12-14nm,IL-1β的直径约为 4.5nm,完全可以使得其通过。因此,推测该孔道是 IL-1β分泌至细胞外的重要途径。
最近,邵峰院士的团队又在细胞焦亡研究领域取得了新的突破,揭示了另一种Gasdermin家族蛋白GSDME引起细胞焦亡的机制。这一发表在《自然》杂志上的发现对癌症治疗(尤其是化疗)的研究和开发具有重要指导意义。不同于GSDMD,GSDME仅能被caspase-3所切割,释放出可导致细胞膜穿孔的N端片段。Caspase-3则可被肿瘤坏死因子-α(TNFα)或化疗药物所激活,引起细胞凋亡;如果此时细胞中也存在GSDME蛋白,则会使细胞从凋亡迅速转入焦亡的进程,或者直接走向细胞焦亡。在人体的许多正常细胞中,都会有GSDME蛋白表达。如果对这些表达GSDME的正常细胞施以化疗药物,均会导致细胞焦亡,而caspase的抑制剂zVAD或者GSDME的敲除和敲低则会阻断焦亡的进程。当GSDME敲除的健康小鼠接受化疗药物后,其经历的有害副作用(包括组织损伤和体重减轻等)相比野生型小鼠则会显著减轻。
相比之下,GSDME蛋白在大多数类型的癌细胞中均不表达。不过,GSDME的表达与细胞焦亡之间的关系则是相似的:只有表达了GSDME的癌细胞才会被化疗药物或TNFα诱导进入细胞焦亡。在许多不表达或表达极少GSDME蛋白的癌细胞中,GSDME基因的启动子区域被甲基化,使其处于转录抑制状态。如果对其施以DNA甲基化酶抑制剂decitabine,则会上调GSDME蛋白的水平,增加化疗药物对癌细胞的杀伤力。
这一研究改变了人们对于细胞程序性死亡的理解。Caspase-3长期以来被认为是发生细胞凋亡的标志,而如今则与细胞焦亡的发生也联系在了一起。同时可以看出,由caspase-3和GSDME介导的细胞焦亡机制,对于改进化疗药物的使用效果提供了重要的思路。





2022年10月25日 下午 5:56 沙发
啊实打实