2024年5月8日,来自美国礼来研究实验室Laura F. Michael团队在学术期刊《自然》发表了标题为“Discovery of potent small-molecule inhibitors of lipoprotein(a) formation.”的研究成果,发现脂蛋白(a)形成的强效小分子抑制剂。
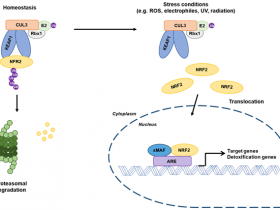
研究人员表示,脂蛋白(a)(Lp(a))是一种独立的心血管风险因子,是由低密度脂蛋白(LDL)颗粒和载脂蛋白(a)(apo(a))相互作用形成的脂蛋白颗粒。apo(a)首先通过Kringle IV(KIV)7和8结构域与LDL上载脂蛋白B-100(apoB-100)的赖氨酸残基结合,然后载脂蛋白(a)和载脂蛋白B-100之间形成二硫键,生成Lp(a)。
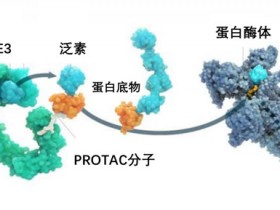
研究人员展示了可以通过小分子与apo(a) KIV7-8的相互作用来抑制Lp(a)形成的第一步。研究人员发现了能与apo(a) KIV7-8结合的化合物,通过化学优化和进一步应用多价性,研究人员创造出了具有亚纳摩尔效力的化合物,可抑制Lp(a)的形成。口服原型化合物和一种强效多价干扰素LY3473329(muvalaplin)可降低转基因小鼠和猴体内的Lp(a)水平。

c,LY3473329的化学结构; d,LY3473329的晶体结构
虽然多价分子能与大鼠纤溶酶原的Kringle结构域结合并降低纤溶酶原的活性,但纤溶酶原序列的物种选择性差异表明,抑制剂分子会降低人类Lp(a)的水平,但不会降低纤溶酶原的水平。这些数据支持了LY3473329的临床开发,目前该药已进入2期研究,这是一种降低Lp(a)水平的强效特异性口服药物。
文章来源:
Diaz, Nuria, Perez, Carlos, Escribano et al, Discovery of potent small-molecule inhibitors of lipoprotein(a) formation.DOI: 10.1038/s41586-024-07387-z, Nature:最新IF:69.504