1、Cell Metabolism: 10小时限时饮食可以降低代谢综合征患者的体重、血压和致动脉粥样硬化性脂质
近日,来自美国加州大学圣地亚哥分校Pam R. Taub和索尔克生物研究所Satchidananda Panda研究组在《细胞—代谢》上发表了题为“Ten-Hour Time-Restricted Eating Reduces Weight, Blood Pressure, and Atherogenic Lipids in Patients with Metabolic Syndrome.”的研究论文,发现10小时限时进食可以降低代谢综合征患者的体重、血压和致动脉粥样血脂。
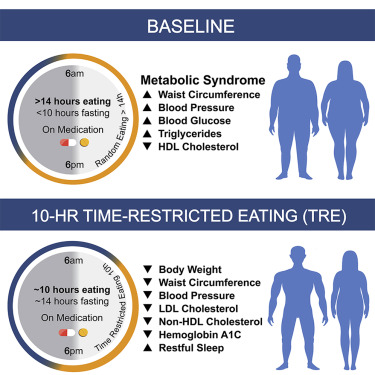
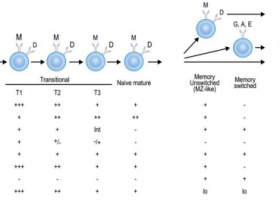
Fig 1.来源 Cell Metabolism
在一项单组配对样本的试验中,19名患有代谢综合征并且其基线平均每日进食时间≥14小时的参与者,接受了持续12周的10小时限时饮食(TRE)(所有饮食在自我选择的10小时窗口内完成),其中大部分患者接受了他汀类和/或降压治疗。研究发现,这种TRE干预可改善代谢综合征患者接受标准药物治疗(包括高他汀类药物和抗高血压药物的使用)的心脏代谢健康。TRE可能是一种强大的生活方式干预措施,可以添加到标准的医学实践中以治疗代谢综合征。
据介绍,在动物模型中,限时喂养(TRF)可以预防和逆转代谢疾病。在人体试验中,限时饮食(TRE)降低了健康人群的代谢疾病风险。然而,代谢综合症患者经常接受药物治疗,并且从未在动物模型或人类中测试过TRE是否可以与药物治疗协同发挥作用。线粒体丙酮酸载体调控肿瘤发生。
(评论: 10小时内进食,另14小时禁食,夜宵是完全不能吃了)
文章来源:
Michael J. Wilkinson et al, Ten-Hour Time-Restricted Eating Reduces Weight, Blood Pressure, and Atherogenic Lipids in Patients with Metabolic Syndrome. Cell Metabolism, DOI: 10.1016/j.cmet.2019.11.004, 最新IF:22.415
2、Nature Genetics: 数千种CRISPR扰动引起的增强子-启动子调控的接触活动模型
近日,来自MIT-哈佛大学博德研究所Jesse M. Engreitz、Eric S. Lander等研究人员在《自然—遗传学》杂志上发表了题为“Activity-by-contact model of enhancer–promoter regulation from thousands of CRISPR perturbations.”的合作成果。他们利用新研发的技术,建立了数千种CRISPR扰动引起的增强子-启动子调控的接触活动模型。
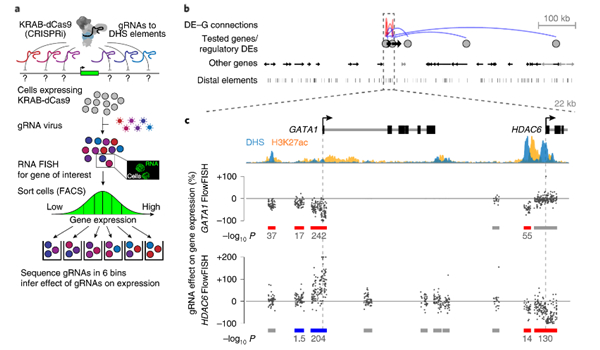
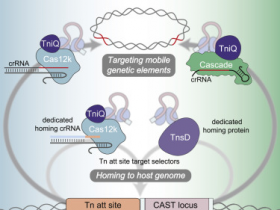
Fig. 2 | CRISPRi-FlowFISH identifies regulatory elements for GATA1 and HDAC6.
研究人员开发了一种叫做CRISPRi-FlowFISH实验方法来打乱基因组中的增强子,并将其用于测试30个基因中的超过3500个潜在增强子与基因的连接。
研究人员发现一个简单的接触活动模型在预测CRISPR数据集中的复杂连接方面远胜过先前的方法。通过接触活动模型,研究人员可以在染色质状态测量的基础上,构建特定细胞类型中增强子与基因的连接的全基因组图谱。
CRISPRi-FlowFISH和接触活动模型共同提供了一种系统的方法来定位和预测哪些增强子调节哪些基因,并将有助于解释非编码基因组中数千种疾病风险变体的功能。
据了解,人类基因组中的增强子元件可控制基因在特定细胞类型中的表达方式,并包含成千上万的遗传变异,这些变异会影响常见疾病。然而,人们仍然不知道增强子如何调控特定基因,并且缺乏通用规则来预测不同细胞类型的增强子与基因的连接。
(评论:厉害 学习了 )
文章来源:
Charles P. Fulco et al, Activity-by-contact model of enhancer–promoter regulation from thousands of CRISPR perturbations. Nature Genetics, 最新IF:25.455
3、Science: 通过工程化B细胞成熟,实现针对性地选择HIV特异性抗体突变
近日,来自美国杜克大学医学院Kevin O. Saunders、Barton F. Haynes与哈佛医学院Frederick W. Alt等研究人员在《科学》上发表了题为“Targeted selection of HIV-specific antibody mutations by engineering B cell maturation”的研究论文,通过工程化B细胞成熟,实现针对性地选择HIV特异性抗体突变。
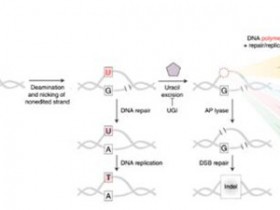
研究人员在人bnAb前体敲入小鼠和接种了旨在选择不可能突变免疫原的野生型猕猴中引发了血清中和HIV-1抗体。研究人员设计了两个HIV-1包膜免疫原,它们结合CD4结合位点或V3-聚糖bnAb谱系的前体B细胞。在体外,一旦前体获得所需的不可能突变,这些免疫原就与bnAb前体更牢固地结合。用针对CD4结合位点的免疫原诱导的猕猴接种CD4结合位点的血清中和抗体。在人bnAb前体敲入小鼠中引发的抗体序列编码了对bnAb发育至关重要的功能性不可能突变。在bnAb前体敲入小鼠中,研究人员分离出了一种疫苗引发的单克隆抗体,其带有功能不大可能的突变,并能够中和多个HIV-1全局隔离株。bnAb前体、bnAb和疫苗引发的抗体的结构揭示了获得不可识别的突变在识别HIV-1包膜中发挥的确切作用。因此,这一免疫原在猕猴和敲入小鼠中引起抗体反应,表现出新生的广泛中和抗体的突变模式、结构特征或中和谱。
(评论: 更有效的HIV抗体)
文章来源:
Kevin O. Saunders et al, Targeted selection of HIV-specific antibody mutations by engineering B cell maturation. Science,DOI: 10.1126/science.aay7199, 最新IF:41.037