1、Nature:CXC趋化因子受体2激活和信号传导的结构基础
2020年7月1日,来自上海科技大学刘志杰、华甜等研究人员在《自然》杂志上合作在发表了题为“Structural basis of CXC chemokine receptor 2 activation and signaling.”的研究论文,解析了CXC趋化因子受体2激活和信号传导的结构基础。
研究人员报道了白细胞介素8(IL8,也称为CXCL8)激活的人类CXC趋化因子受体2(CXCR2)与Gi蛋白复合的冷冻电镜结构,以及设计的变构拮抗剂结合的CXCR2晶体结构。这些结果揭示了CXCL8和CXCR2之间以及CXCR2–Gi蛋白相互作用的独特的浅层结合模式。对CXCR2的非活跃状态和活跃状态的进一步结构分析揭示了一个独特的激活过程以及趋化因子受体的竞争性小分子拮抗作用。
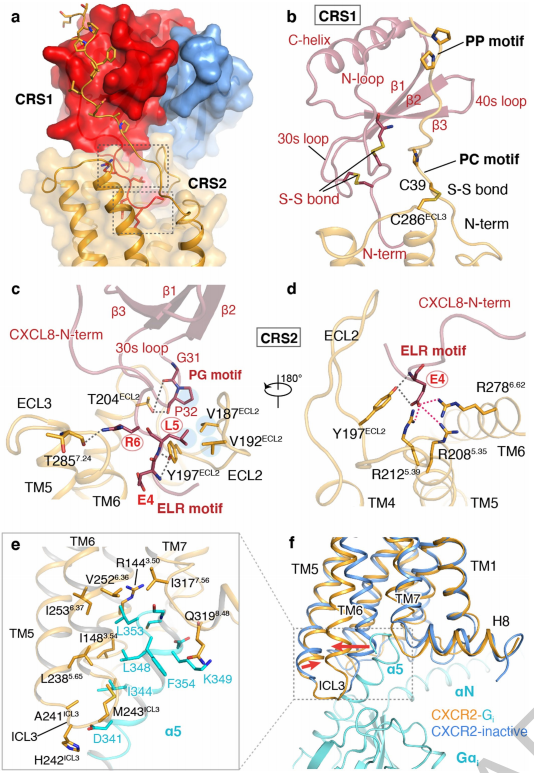
Fig 1.nature截图 | Interactions of CXCR2 with CXCL8 and Gi protein
此外,这项研究为内源性蛋白质分子如何激活G蛋白偶联受体(GPCR)提供了新见解,这将有助于开发靶向趋化因子系统的疗法,从而获得更好的药理作用。
据介绍,趋化因子及其受体介导细胞迁移,从而影响多种基本的生物学过程和疾病状况,例如炎症和癌症。尽管已经对趋化因子受体的结构研究和受体-趋化因子识别进行了充分研究,但对内源性趋化因子诱导的受体激活和G蛋白偶联的了解还很少。
(评论:揭示了新型冠状病毒聚合酶复合体催化过程中“转位前”和“转位后”两个生理状态的构象特征。)
文章来源:
Kaiwen Liu, Lijie Wu et al, Structural basis of CXC chemokine receptor 2 activation and signaling. DOI: 10.1038/s41586-020-2492-5, Nature:最新IF:43.07
2、Nature:随着年龄的增长,血脑屏障会随年龄变化而受损
2020年7月1日,来自美国斯坦福大学医学院Tony Wyss-Coray小组在《自然》的上发表了标题为“Physiological blood–brain transport is impaired with age by a shift in transcytosis.”的研究成果,发现生理性血脑运输会随着年龄的增长受到损害。
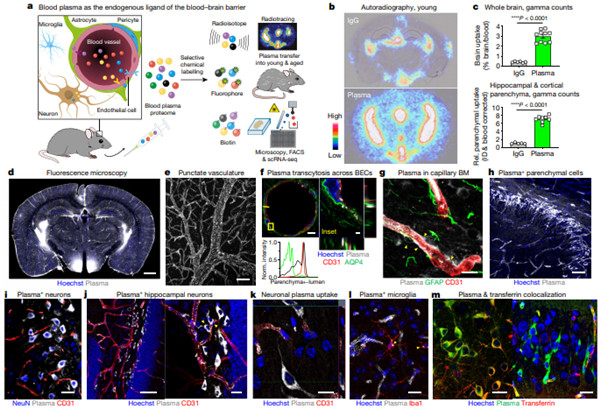
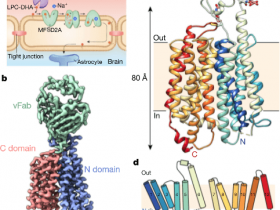
Fig 2. nature截图 | Circulatory proteins permeate the healthy adult brain
研究人员标记了构成小鼠血浆蛋白质组的数百种蛋白质,并且在其全身性给药后,研究了血脑屏障(BBB)及其生理配体。研究人员发现血浆蛋白很容易渗入健康的脑实质,并由BBB特异性转录程序维持转运。与IgG抗体不同,血浆中蛋白质的摄取在衰老的大脑中减少,这是由与年龄相关的从配体特异性受体介导的转运到非特异性转胞吞作用。
这种与年龄有关的转变与周细胞覆盖率的特定损失同时发生。随年龄上调的磷酸酶ALPL(一种预测的转运负调节因子)的药理抑制作用可增强大脑对治疗相关的转铁蛋白、转铁蛋白受体抗体和血浆的摄取。
这些发现揭示了生理蛋白转入健康大脑的程度,一种随着年龄增长而广泛产生血脑屏障功能障碍的机制,以及一种增强药物传递的策略。
据了解,大脑的血管界面被称为BBB,其参与维持大脑功能,部分是通过其较低的跨细胞渗透性。然而,最近的研究表明,大脑衰老对循环蛋白敏感。因此,目前尚不清楚个别注射的外源示踪剂的渗透性是否完全代表了血脑转移能力。
(评论:这个让我们对血脑屏障有重新的认识,不再是静态的屏障)
文章来源:
Andrew C. Yang, Marc Y. Stevens et al, Physiological blood–brain transport is impaired with age by a shift in transcytosis. DOI: 10.1038/s41586-020-2453-z. Nature:最新IF:43.07
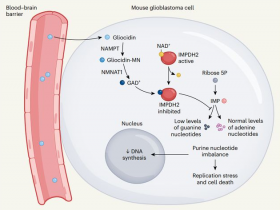
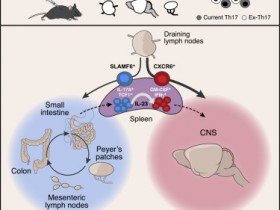
2020年7月1日,来自美国纽约大学医学院Dan R. Littman、Lin Wu等研究人员合作在《细胞》上发表了标题为“Niche-Selective Inhibition of Pathogenic Th17 Cells by Targeting Metabolic Redundancy.”研究成果,发现靶向代谢冗余能够选择性抑制致病性Th17细胞。
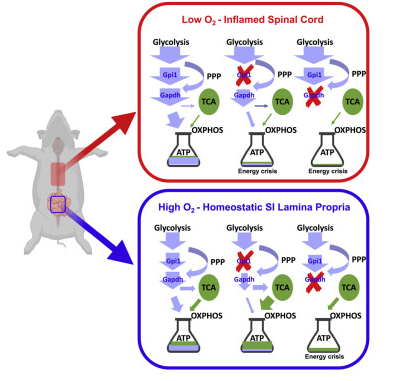
Fig 3. CELL截图 | Gpi1在不同环境中的选择性冗余提供了特异性抑制致病性Th17细胞的方法。
研究人员发现,CRISPR介导的小鼠T细胞糖酵解靶向导致Th17细胞整体丢失,而糖酵解酶葡萄糖磷酸异构酶(Gpi1)的缺乏选择性地消除了致脑炎性和致大肠杆菌性Th17细胞,而基本上不影响稳态微生物群特异性Th17细胞。在稳态的Th17细胞中,Gpi1失活后的糖酵解部分阻滞被磷酸戊糖途径流和线粒体呼吸增加所补偿。相反,炎性Th17细胞会经历低氧的微环境,已知这种环境会限制线粒体呼吸,这与Gpi1的丧失不相容。
这项研究表明,以Gpi1为靶点抑制糖酵解可能是一种有效的治疗策略,对Th17介导的自身免疫性疾病的毒性最小,而且可以将代谢冗余用于疾病过程的选择性靶向。
据了解,由于其关键的基础作用,靶向糖酵解被认为在治疗上是难以对付的。但是,目前尚未完全探讨单个糖酵解步骤的背景相关需求。
(评论:首次报道了可以特异性抑制致病性Th17细胞的方法,病情这种方洧可能不会产生巨大的毒副作用。)
文章来源:
Lin Wu, Kate E.R. Hollinshead et al, Niche-Selective Inhibition of Pathogenic Th17 Cells by Targeting Metabolic Redundancy. DOI: 10.1016/j.cell.2020.06.014,Cell:36.216