2024年3月27日,来自中国科学院上海有机化学研究所Daichao Xu小组在学术期刊《自然—细胞生物学》发表了标题为“Defective prelamin A processing promotes unconventional necroptosis driven by nuclear RIPK1.”的研究成果,发现核纤层蛋白A加工缺陷促进由核RIPK1诱导的非典型坏死。
据介绍,由ZMPSTE24基因功能缺失突变引起的核纤层蛋白A加工酶缺陷,是一系列以法尼基化前核纤层蛋白A积累为特征的早衰症的病因。
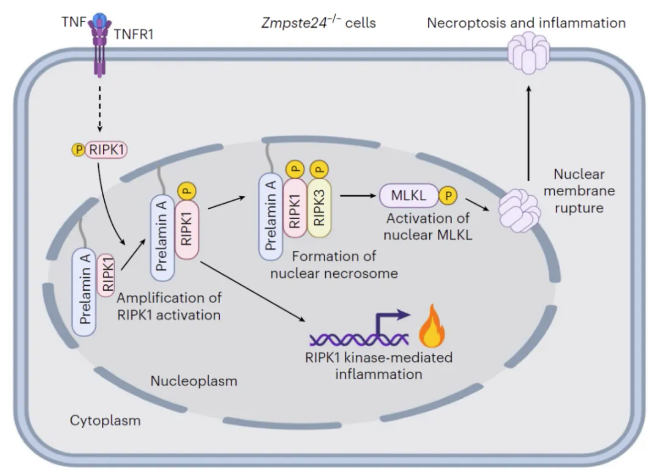
毒性蛋白prelamin A启动的由核RIPK1介导的非典型细胞核程序性坏死途径的机制模式图
研究人员发现,在ZMPSTE24缺陷细胞中,累积的前核纤层蛋白A会招募RIPK1至细胞核,以促进其在肿瘤坏死因子刺激下的激活。然后,激酶激活的RIPK1在细胞核中促进RIPK3介导的MLKL激活,导致核膜破坏和细胞坏死。这种信号传导依赖于前核纤层蛋白A的法尼基化,法尼基化将前核纤层蛋白A固定在核膜上,作为坏死的成核平台。
遗传性坏死凋亡可改善Zmpste24-/-小鼠的早衰表型。该研究结果确定了一种由ZMPSTE24缺乏导致的非典型核坏死途径,它在类早衰症中具有致病性,该研究表明RIPK1是治疗前核纤层蛋白A相关类早衰症的潜在靶点。
文章来源:
Yang, Yuanxin, Zhang, Jian, lv, Mingming et al ,Defective prelamin A processing promotes unconventional necroptosis driven by nuclear RIPK1.DOI: 10.1038/s41556-024-01374-2,Nature Cell Biology:最新IF:28.213