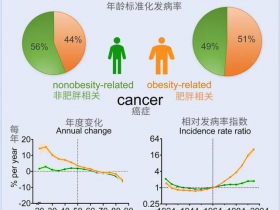
1、NATURE:使用CRISPR-CAS9筛选确定癌症治疗目标的优先
近日Behan FM等研究人员在NATURE上发表了题为“使用CRISPR-CAS9筛选确定癌症治疗目标的优先级”的文章,敲掉了横跨30个癌种的324种癌细胞系中的18,009个基因,并开发了数据驱动的框架,以优先考虑癌症治疗的候选者。
功能基因组学方法可以克服研究中的一些限制,例如缺乏对强健靶标的鉴定和较差的临床疗效。这些限制一直阻碍着癌症药物的开发。
研究人员将细胞适应性效应与基因组生物标记物和用于药物开发的目标易处理性相结合,以系统地优先定义组织和基因型中的新靶标。此外,研究人员验证了最有希望的依赖性之一,Werner综合征ATP依赖性解旋酶,作为具有微卫星不稳定性的多种癌症类型肿瘤的合成致死靶标。

使用CRISPR-CAS9筛选确定癌症治疗目标的优先
研究人员的分析提供了癌症依赖性的资源,生成了优先考虑癌症药物目标的框架,并提出了具体的新目标。
该研究中描述的原则可以为药物开发的初始阶段提供信息,为新的,多样化的,和更有效的癌症药物目标组合做出贡献。
(评论:敲掉了横跨30个癌种的324种癌细胞系中的18,009个基因,这工作量也是佩服。。。)
原始出处:
Behan FM et al. Prioritization of cancer therapeutic targets using CRISPR-Cas9 screens. NATURE, 2019; doi: 10.1038/s41586-019-1103-9.
2、NATURE:WRN解旋酶是微卫星不稳定癌症的合成致死靶标
近日,Broad Institute等研究人员在题为“WRN helicase is a synthetic lethal target in microsatellite unstable cancers[J]”的文章,研究结果表明,WRN是一种合成致死的脆弱性,是MSI癌症的有希望的药物靶标。
合成致死率是两个遗传事件之间的相互作用,通过这两个遗传事件共同发生导致细胞死亡,但每个事件本身都没有导致细胞死亡的能力。其可以用于癌症治疗。
DNA修复过程代表了有吸引力的合成致死靶标,因为许多癌症表现出DNA修复途径的损伤,这可能导致对特定修复蛋白的依赖。
聚(ADP-核糖)聚合酶1(PARP-1)抑制剂在治疗同源重组缺陷的癌症中的成功突出了这种方法的潜力。
假设其他DNA修复缺陷会产生合成致死关系,研究人员通过微卫星不稳定性(MSI)查询癌症中的依赖性,这是由于DNA错配修复不足造成的。
研究人员使用CRISPR-Cas9介导的敲除和RNA干扰,分析了来自大规模沉默筛选的数据,并发现RecQ DNA解旋酶WRN在体外和体内MSI模型中是选择性必需的,但在微卫星稳定癌症模型中是可有可无的。

WRN解旋酶是微卫星不稳定癌症的合成致死靶标
在MSI模型中,WRN的消耗诱导双链DNA断裂,并促进细胞凋亡和细胞周期停滞。 MSI癌症模型需要WRN的解旋酶活性,但不需要其外切核酸酶活性。
(评论:WRN的出现,对很多携带MSI的癌症患者的治疗带来了新希望。)
原始出处:
Edmond M. Chan, Tsukasa Shibue, James M. McFarland, et al. WRN helicase is a synthetic lethal target in microsatellite unstable cancers[J]. Nature, 2019. DOI:10.1038/s41586-019-1102-x.
3、NATURE:破骨细胞的发育起源、功能维持和基因拯救
最近Jacome-Galarza CE等研究人员在《Nature》上发表题为“破骨细胞的发育起源、功能维持和基因拯救”的文章,研究结果确定了破骨细胞的发育起源和控制其在出生后骨骼维持的机制。
破骨细胞是多核巨细胞,可以再吸收骨骼,确保骨骼和骨髓造血生态位的发育和持续重塑。已有的研究显示,破骨细胞活性缺陷导致骨硬化和骨髓衰竭,而过量活动可导致骨质流失和骨质疏松症。
骨质疏松症可以通过骨髓移植在人和小鼠中得到部分治疗,与破骨细胞的造血起源一致,并且,研究表明,它们通过在CSF1和RANK配体存在下融合来自造血干细胞的单核细胞前体而发展。
然而至今为止,破骨细胞的发育起源和寿命,以及确保在整个体内维持破骨细胞功能的机制仍然很大程度上未被探索。
最近,研究人员发现,定植胎儿骨化中心的破骨细胞来源于胚胎红细胞 - 骨髓祖细胞。这些红细胞 - 骨髓祖细胞衍生的破骨细胞是正常骨发育和牙齿萌出所必需的。然而,在新生小鼠中及时输注造血干细胞来源的单核细胞足以挽救早发性常染色体隐性骨质疏松症中的骨发育。
研究人员还发现,破骨细胞,骨量和骨髓腔的出生后维持涉及循环血液单核细胞与长寿命破骨细胞合胞体的迭代融合。因此,单核细胞的共生或输血可以导致在没有造血干细胞嵌合体的情况下,破骨细胞中的长期基因转移,并且可以挽救由组织蛋白酶K缺乏引起的成人发病的骨硬化表型。
(评论:这些数据提出了拯救骨硬化病中破骨细胞缺乏和调节体内破骨细胞活性的策略。)
原始出处:
Jacome-Galarza CE et al. Developmental origin, functional maintenance and genetic rescue of osteoclasts. NATURE, 2019; doi: 10.1038/s41586-019-1105-7.