华中科技大学同济医学院的研究人员提出MHC II在BCP中的调控机制,通过研究MHC II的变化来考证。作者认为调节脊髓小胶质细胞中MHC II的表达以抑制适应不良的神经免疫反应可能是疼痛缓解的潜在治疗策略。骨癌痛机制详细图文为你答疑!
俗话说,牙痛不是病,痛起来要人命。医学上定义疼痛(pain)是一种复杂的生理心理活动,是临床上最常见的症状之一。它包括伤害性刺激作用于机体所引起的痛感觉,以及机体对伤害性刺激的痛反应(躯体运动性反应和/或内脏植物性反应,常伴随有强烈的情绪色彩)。痛觉可作为机体受到伤害的一种警告,引起机体一系列防御性保护反应。但另一方面,疼痛作为报警也有其局限性(如癌症等出现疼痛时)。
今年2月,Brain, Behavior, and Immunity杂志出版了华中科技大学同济医学院田玉科教授课题组名为STAT1 as a downstream mediator of ERK signaling contributes to bone cancer pain by regulating MHC II expression in spinal microglia的文章,该文章阐述了骨癌痛的相关机制。
许多恶性肿瘤会导致严重的癌症诱导的骨痛,而骨癌痛的机制目前人不是很清楚,这使得对骨癌痛(bone cancer pain, BCP)的治疗也不是很理想。许多关于脊髓背小神经胶质细胞的影响的研究表明MHC II可能是慢性神经性疼痛和自身免疫性疾病中的关键分子,因此,作者认为调节脊髓小胶质细胞中MHC II的表达以抑制适应不良的神经免疫反应可能是疼痛缓解的潜在治疗策略。因此,作者研究了MHC II在BCP中的作用。
在作者2015年的研究中发现,ERK信号通路参与了BCP的发病机制,而已有研究表明ERK信号通路的激活加强STAT1磷酸化。有意思的是,STAT1信号通路是通过调节II类反式激活因子(CIITA)的表达的MHC II表达的关键调节剂。因为,作者在研究中特别的分析了在调节MHC II表达的信号通路中,ERK和STAT1之间的关系。
作者通过大鼠BCP模型展开研究,从多方面入手阐述BCP的机制。对BCP模型进行的放射性研究显示,在同侧胫骨(红色箭头)的近端骨会出现时间依赖性溶骨性破坏的迹象,一些癌细胞也在第21天从胫骨腔迁移出并损伤外周软组织。 而HE染色切片显示正常骨髓细胞被接种的Walker 256癌细胞代替,并且健康的骨结构从第14天开始消失。而作为伤害性感受阈的压力-缩腿阈(Paw-Withdrawal Threshold, PWT)测试结果显示BCP实验组的PWT持续恶化。这些实验结果说明Walker 256癌细胞的接种会诱导胫骨骨溶解和机械性异常性疼痛。
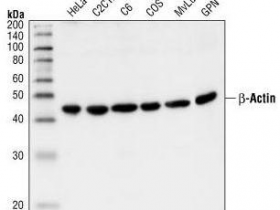
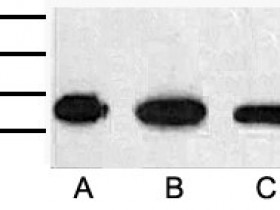
Western Blot 结果显示,在接种Walker 256癌细胞后,会显着诱导CIITA和MHC II RT1B的表达,在第14天达到检测最大值。双免疫荧光染色显示,在Walker 256癌细胞接种14天后,BCP大鼠的浅表脊髓背角中MHC II RT1B(红色)与Iba1(绿色)阳性细胞共表达。用层板计数Iba1和MHC II RT1B双阳性细胞的数目,发现其在BCP后14天急剧增加直到观察结束。

而对BCP模型小鼠进行PWT等测试显示,BCP大鼠在手术第7天,其机械性缩足阈值(PWT)从基线12.38±1.34g降低至4.05±1.68g,并持续至第14天。与生理盐水(NS)相比,二甲胺四环素(MC)能有效地改善机械性异常性疼痛的发展并抑制MHC II RT1B的上调。这说明MHC II介导BCP的机械性异常疼痛。

此外,在BCP大鼠中STAT1的mRNA水平和蛋白水平都显著上调,但总STAT1和磷酸化STAT1的蛋白水平有着明显差异。从共聚焦结果来看,pSTAT1 ser727与Ibal和GFAP共定位,不与NeuN共定位。

相似的,在BCP大鼠中ERK的磷酸化显著增强。进一步研究发现,ERK信号会调节STAT1的磷酸化,并且pSTAT1在BCP条件下调节脊髓中MHC II的表达。

Western Blot结果显示,在BCP大鼠脊髓中,AG490会显著增加pSTAT1 ser727水平,而Fludarabine和U0126则显著抑制pSTAT1 ser727,CIITA以及MHC II RT1B水平。此外,U0126还显著抑制pERK水平。

但是,在加入重组大鼠IFNγ后的Western Blot结果显示,AG490对pSTAT1 ser727的影响被抑制,而Fludarabine和U0126则仍旧显著抑制pSTAT1 ser727,CIITA以及MHC II RT1B水平。此外,U0126还显著抑制STAT1和pERK水平。这些证据表明,在BCP大鼠模型中,ERK信号会调节STAT1的磷酸化,并且pSTAT1在BCP条件下调节脊髓中MHC II的表达。

由此,作者提出来MHC II在BCP中的调控机制——胞外刺激激活ERK信号通路导致STAT1的磷酸化激活,促使CIITA上调,进一步使得MHC II RT1B水平上调,并最终导致骨癌痛。
骨癌痛机制待你进一步的研究考证,目前研究较多的疼痛,大多是离子通道异常或癌症引起的。当然,本身癌症中就有会引起离子通道异常的现象。对疼痛产生的机制做更深入的研究,有助于丰富治疗措施,从而改善患者的生活质量、身体机能。而对疼痛机制的研究,好的研究工具必不可少。像文章中提到的Jackson荧光二抗、ERK/STAT1信号通路研究所需抗体&抑制剂之类的自不必说,艾美捷在以往的品牌产品介绍中已然推介过多次,Jackson、cayman、AAT都是全球知名品牌,产品齐全,质量有保障。所谓酒香不怕巷子深,此处便不再赘叙。艾美捷今日借此要给诸位推荐的是合作伙伴Alomone公司提供的疼痛相关研究抗体。
Alomone是位于以色列的全球著名离子通道相关产品供应商,他们的抗体经过严格设计,保证最大的免疫亲和以及无交联反应性。每支抗体还提供免费的抗原作为质控对照。目前Alomone有包括TRPV2,Cannabinoid Receptor,Ca/Na/K离子通道以及Nicotinic Acetylcholine Receptor在内的179款与疼痛相关的产品,更多产品还在继续研发中。同时,艾美捷也为大家推
荐一款神经元示踪剂,这款示踪剂产自艾美捷的新的合作伙伴,著名的生物标记检测产品供应商Vectorlabs。艾美捷致力为广大科研小伙伴提供最全面最优质的科研工具,了解更多产品信息,欢迎与我们联系。
| 产品名称 | 货号 | 详情 |
| Anti-TRPV1 | ALO-ACC-030-50 | 详情 |
| Anti-Cannabinoid Receptor 1 (extracellular) | ALO-ACR-001-50 | 详情 |
| Anti-CaV3.1 | ALO-ACC-021-50 | 详情 |
| Anti-KV4.2 | ALO-AGP-038-50 | 详情 |
| Anti-NaV1.1 | ALO-AGP-043-50 | 详情 |
| Anti-Nicotinic Acetylcholine Receptor alpha6 (extracellular) | ALO-ANC-006-50 | 详情 |
| NEUROBIOTIN Tracer | SP-1120 | 详情 |