1、Cell:重磅!找到了流感病毒的致命弱点
近日,美国NIH国家过敏和传染病研究所在Cell杂志上发表了题为“A site of vulnerability on the influenza virus hemagglutinin head domain trimer interface”的研究报告,表明流感病毒蛋白质的不断变化的“头部”具有意想不到的致命弱点。发现并鉴定了一种天然存在人体抗体中的结构,该抗体可以识别和破坏病毒进入机体、感染细胞的一部分血凝素(HA)蛋白。
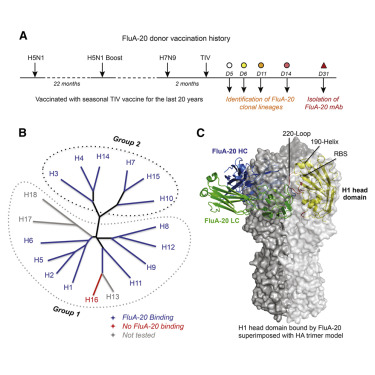
(图片来源:Cell)
研究人员从接种过许多流感疫苗的人体那里分离出FluA-20抗体。通过在一系列实验,发现FluA-20可以“进入”HA三聚体分子中难以接近的部分,并使其分解,从而防止病毒从细胞传播到细胞。
这一发现令人感到惊讶,因为这个三聚体HA区域被认为是稳定的,而且不能被抗体接近。此外,这个区域与HA头部的其它部位不同,出现变化的几率很小,在毒株之间保守性强。因此理论上,针对该精确区域,基于抗体的治疗剂将对许多甲型流感病毒株有效。同样,引发针对该靶标的抗体的疫苗可以提供针对任何流感病毒株的长期保护,可以减少每年季节性流感疫苗接种的需要。
在小鼠研究中,研究人员发现当小鼠接触导致人类疾病四种不同甲型流感病毒亚型时,FluA-20可以预防感染或疾病发生。实验中使用的两种病毒H1N1和H5N1是第1组流感亚型,而另外两种,H3N2和H7N9是第2组的成员。目前的流感疫苗必须含有来自两种亚型的病毒组分,帮助引发匹配的抗体。能够产生针对两组成员的有效抗体的单一疫苗可以提供广泛的多年抗流感保护。
(评论:预防流感又有新的可行办法了。)
文章来源:
Bangaru S, Lang S, Schotsaert M, et al. A site of vulnerability on the influenza virus hemagglutinin head domain trimer interface. Cell. 2019 May 16;
2、Cell:非酒精性脂肪肝病或找到新靶点
近日,西班牙巴塞罗那科学技术学院的研究团队在cell杂志上发表了题为“Deficient Endoplasmic Reticulum-Mitochondrial Phosphatidylserine Transfer Causes Liver Disease “的文章,发现了一种能够缓解NASH症状的蛋白。
NASH患者的肝脏不但出现脂肪堆积,而且产生炎症。在这项研究中,研究人员通过对NASH患者肝脏样本的分析,发现这些患者肝细胞中一种名为mitofusin 2(Mfn2)的线粒体蛋白水平显著下降。而且他们在小鼠的NASH模型中同样发现Mfn2水平显著下降。那么Mfn2与NASH的疾病发生是不是有什么关系?
为了确认Mfn2蛋白的功能,研究人员在肝脏中敲除了Mfn2基因。他们发现敲除Mfn2能够在小鼠模型中促进炎症的发生,提高甘油三酯积累,促进肝纤维化和肝癌的发生。而当研究人员用AAV病毒载体在小鼠肝脏中提高Mfn2蛋白的表达后,他们发现小鼠NASH症状得到减轻。这表明,Mfn2蛋白有改善NASH症状的作用。
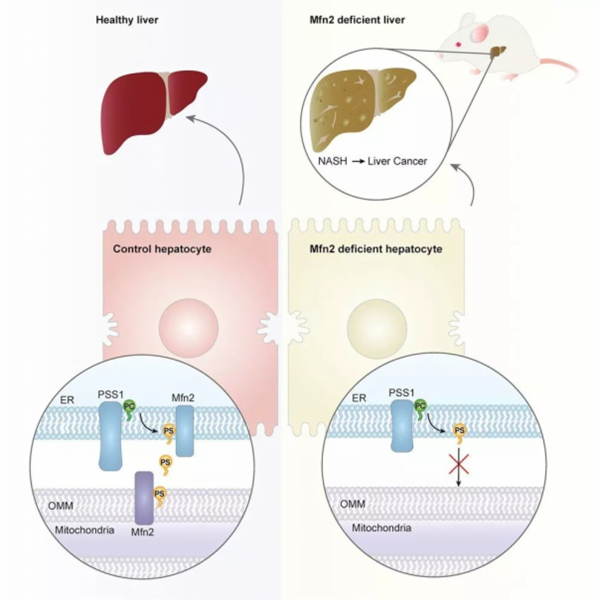
(图片来源:cell)
进一步研究表明,Mfn2蛋白能够与磷脂酰丝氨酸(PS)结合,促进PS进入线粒体和帮助磷脂酰乙醇胺(PE)的合成。肝脏Mfn2蛋白缺失会导致PS运输和磷脂合成水平下降,引发内质网应激反应和与NASH相似的症状和肝癌。这一研究揭示了NASH发病的一条新机制。
(评论:这项研究有望预防非酒精性脂肪肝)
文章来源:
Hernández-Alvarez MI, Sebastián D, Vives S, et al. Deficient Endoplasmic Reticulum-Mitochondrial Phosphatidylserine Transfer Causes Liver Disease. Cell. 2019 May 2;
3、Cell:HIV疫苗递送策略可增强保护性的免疫反应
近日,来自拉霍亚免疫学研究所的科学家等人员在Cell上发表了题为““的文章,发现在一段时间内以小剂量递送HIV疫苗会比同时接种同一种疫苗时产生更强的免疫反应。
当你生病时,你的免疫细胞会组队清除病原体。可以产生抗体的细胞——B细胞移动到淋巴结中称为生发中心的部位。制造最有希望抗体的B细胞然后进一步的突变,测试和抗体筛选(antibody refinement)。为了击败HIV,B细胞产生的抗体与病毒上的机器结合,引发感染。但艾滋病病毒是一个强硬的对手:它的外部蛋白质外壳可被抗体识别,发散迷惑免疫系统的诱饵。B和TFH细胞致力于靶向诱饵位点,没有意识到抗体会失败。
研究人员利用最近在Crotty实验室研发的一项新技术,从淋巴结中反复提取小样本的生发中心细胞。这让他们实时看到发生的抗体细化,同时保持淋巴结完整,持续改善生发中心的B细胞反应。
研究人员测试了三种免疫策略:一种传统的疫苗,其中疫苗是一次性注射;一种是渗透性迷你药泵技术(osmotic mini-pump technology),这有点像定时释放药丸缓慢地递送疫苗;第三种是逐步增加的剂量策略,其中每隔一天给予动物部分剂量的疫苗,持续12天。
缓释策略似乎使更多B细胞活化更长时间,使它们有时间使用TFH细胞改善抗体强度和结合。随着时间的推移,这些B细胞实际上开始产生中和抗体,这些抗体可以与HIV结构的重要部分结合。
(评论:换一种递送方式就可以增强艾滋病毒疫苗效果、看来攻克艾滋病指日可待了)
文章来源:
Cirelli KM, Carnathan DG, Nogal B, et al. Slow-Delivery Immunization Enhances HIV-Neutralizing Antibody and Germinal Center Responses via Modulation of Immunodominance. Cell. 2019 May 16