1、Nature Genetics:绘制皮层下大脑结构的遗传图谱
近日,来自荷兰伊拉斯谟医学中心M. Arfan Ikram和美国得克萨斯大学圣安东尼奥健康中心Claudia L. Satizabal等研究人员在《Nature Genetics》上发表了题为” Genetic architecture of subcortical brain structures in 38,851 individuals”的研究文章,描绘了38851名个体皮层下大脑结构的遗传结构。
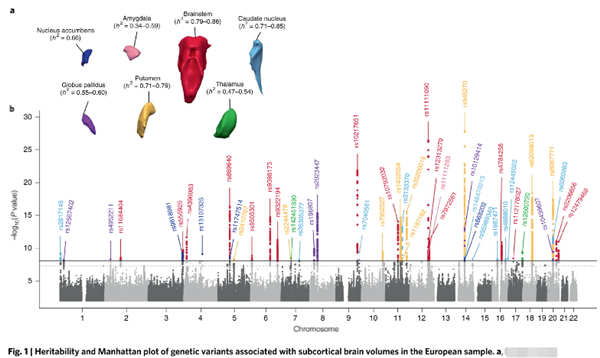
研究人员使用CHARGE、ENIGMA和UK Biobank数据库的近40000名个体进行了全基因组关联分析,确定了与伏隔核、杏仁核、脑干、尾状核、苍白球、壳核和丘脑体积相关的常见遗传变异。
研究人员发现皮层下体积的可变性是可遗传的,并确定48个显著相关的基因组(40个在分析时是新的)。利用基因表达、甲基化和神经病理学数据对这些基因座进行注释,研究人员确定了199个基因可能与神经发育、突触信号传导、轴突运输、细胞凋亡、炎症/感染以及对神经系统疾病的易感性有关。这组基因对于与神经发育表型有关的果蝇直系同源物显著富集,表明进化上保守的机制。
这些发现揭示了大脑发育和疾病的新型生物学机制和潜在药物靶标。
据悉,皮层下大脑结构是运动、意识、情绪和学习所不可或缺的。
(评论:学习了)
文字来源:Claudia L. Satizabal et al, Genetic architecture of subcortical brain structures in 38,851 individuals, Nature, 最新IF:25.455, DOI:10.1038/s41588-019-0516-6
2、Nature Genetics:与脑容量相关的基因
近日,来自美国北卡罗来纳大学教堂山分校Hongtu Zhu等研究人员在《Nature Genetics》上发表了题为“Genome-wide association analysis of 19,629 individuals identifies variants influencing regional brain volumes and refines their genetic co-architecture with cognitive and mental health traits.”的研究结果,利用19629名个体的全基因组关联分析确定了影响大脑容量的变异,并利用认知和心理健康特征完善了其遗传结构。
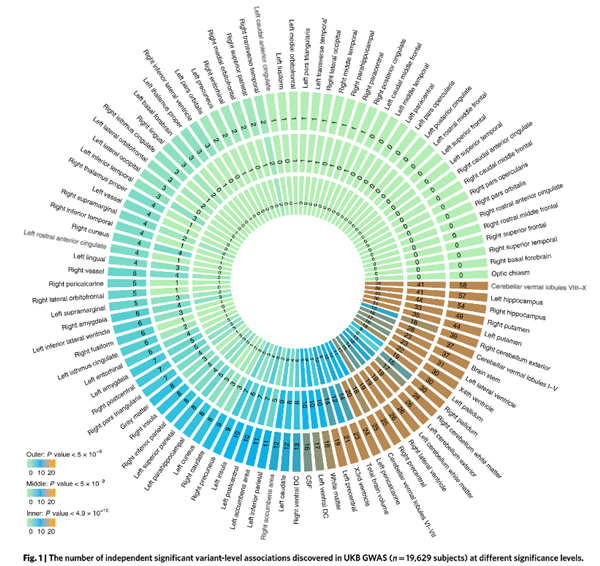
研究人员使用包括19629名参与者的英国生物银行样本,对101种脑容量表型进行了全基因组关联研究(GWAS)。GWAS鉴定了365个独立遗传变体(显著性阈值超过4.9×10−10),并对多种表型进行了相应调整。一项基于基因的关联研究发现了157个相关基因(124个新基因),而功能基因图谱分析将146个其他基因联系在一起。先前发现的许多遗传变异和基因都与认知和心理健康特征有关。通过全基因组多基因风险评分预测,英国生物银行GWAS结果可以解释其他四项独立研究中超过6%的表型变异(P =3.13×10-24)。
总之,这项研究在变体、基因组和基因水平上鉴定了许多新的遗传关联,并加深了我们对大脑体积和其他特征之间的多效性和遗传共构关系的理解。
据了解,人脑的体积变化是可遗传的,并且与许多与脑有关的复杂性状有关。
(评论:人脑真的是一个复杂的系统。)
文章来源:Bingxin Zhao et al ,Genome-wide association analysis of 19,629 individuals identifies variants influencing regional brain volumes and refines their genetic co-architecture with cognitive and mental health traits. Nature Genetics, 最新IF:25.455,DOI:10.1038/s41588-019-0516-6
近日来自西班牙Germans Trias i Pujol大学医院与研究所的Lorenzo Pasquali团队在《Nature Genetics》上发表了题为“The impact of proinflammatory cytokines on the β-cell regulatory landscape provides insights into the genetics of type 1 diabetes.”的研究论文,揭示了促炎细胞因子对β细胞调节作用,并为1型糖尿病(T1D)的发病机制提供了新的见解。
研究人员发现,促炎细胞因子的接触揭示了β细胞调节表观图谱的显著可塑性。通过映射与β细胞转录组、蛋白质组和三维染色质结构变化相关的刺激响应性增强子,研究人员扩展了人类胰岛调节元件的功能。这些数据表明,β细胞对细胞因子的反应是通过诱导新的调控区以及活化调控元件(被胰岛特异性转录因子预先结合)的激活来介导的。研究人员发现,与T1D相关的基因座富含新定位的顺式调控区域,并鉴定了可破坏人类β细胞中细胞因子响应型增强子活性的T1D相关变体。这项研究说明了β细胞如何对促炎环境做出反应,并暗示T1D中刺激响应胰岛增强子的作用。
据介绍,T1D早期阶段的特征是局部自身免疫炎症和胰岛素产生性胰腺β细胞的逐步丢失。
(评论:让我们对促炎细胞因子又有了新的认识。)
文章来源:
Mireia Ramos-Rodríguez et al, The impact of proinflammatory cytokines on the β-cell regulatory landscape provides insights into the genetics of type 1 diabetes. Nature Genetics, 最新IF:25.455,DOI:10.1038/s41588-019-0524-6