Abbikine产品:Dylight 594, Goat Anti-Mouse IgG (A23410, Abbkine,Wuhan, China)
英文名:circKIF4A acts as a prognostic factor and mediator to regulate the progression of triple-negative breast cancer
中文名:circKIF4A作为的预后因素和调节剂来调节三阴性乳腺癌的进展
作者单位:中山大学肿瘤防治中心乳腺肿瘤学系,华南肿瘤学国家重点实验室
研究方向:肿瘤学,肿瘤药物协同创新
杂志名称:Molecular Cancer (2019)
影响因子:9.17
背景
越来越多的研究发现,环状RNA(circRNA)在癌症进展中起着至关重要的作用。但是尚不清楚circRNA在三阴性乳腺癌(TNBC)中的表达特征和功能。
方法
我们使用circRNA微阵列探索TNBC的circRNA表达谱。通过qRT-PCR证实了乳腺癌细胞系和组织中最上调的circRNA,circKIF4A的表达。进行Kaplan-Meier生存分析以分析circKIF4A对TNBC的临床影响。进行了一系列实验以探索circKIF4A在TNBC进程中的功能,例如细胞增殖和迁移。我们研究了circKIF4A对miRNA及其靶基因的调控作用,以探索circKIF4A在TNBC中的潜在调控机制。
结果
qRT-PCR分析证实circKIF4A显着上调并且与TNBC较差的生存呈正相关。 circKIF4A的抑制抑制了TNBC中的细胞增殖和迁移。荧光素酶报告基因测定和RNA免疫沉淀测定表明circKIF4A和KIF4A可以与miR-375结合,并且circKIF4A通过使miR-375海绵化来调节KIF4A的表达。
结论
circKIF4A-miR-375-KIF4A轴通过竞争性内源RNA(ceRNA)机制调节TNBC的进程。因此,circKIF4A可以作为TNBC的预后生物标志物和治疗靶标。
实验结果解析:
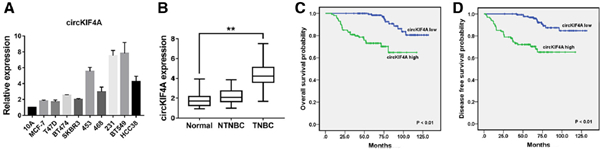
图1 circKIF4A被上调并与TNBC的不良临床结果相关。
A circKIF4A在乳腺癌细胞系中的表达。qRT-PCR显示circKIF4A在TNBC细胞系中上调。
B circKIF4A在乳腺癌组织和正常邻近组织中的表达。**P < 0.01。我们检测了乳腺癌组织和邻近正常组织中的circKIF4A表达,发现TNBC组织中circKIF4A明显上调。
C 240位TNBC患者的OS曲线。D 240名TNBC患者的DFS曲线。我们进行Kaplan-Meier生存分析,发现circKIF4A与TNBC患者生存较差呈正相关。
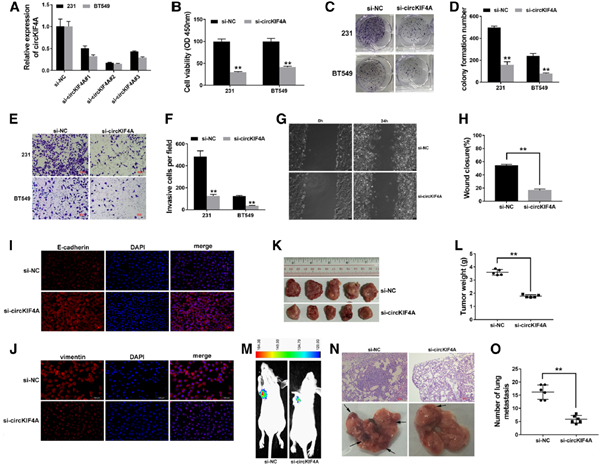
图2 敲除circKIF4A可抑制TNBC的增殖和转移
A si-circKIF4A#2成功地敲除了circKIF4A。为了探索circKIF4A在TNBC中的功能,我们敲低了circKIF4A的表达。 si-circKIF4A#2抑制成功,该实验用于以下实验。
B 用于检测细胞增殖的CCK-8分析。CCK-8分析表明circKIF4A敲低显着抑制细胞增殖。
C 集落形成分析,以检测细胞集落形成能力。D 菌落形成数由Image J定量。circKIF4A敲低还降低了细胞的集落形成能力。
E Transwell测定法以评估细胞迁移能力。F 侵袭性细胞的数量由Image J计算。Transwell分析显示,circKIF4A下调后细胞转移明显减少。
G 伤口愈合试验,以评估细胞迁移能力。H 伤口闭合由Image J计算。伤口愈合试验还显示,敲除circKIF4A可以显着抑制细胞迁移能力
I-J钙粘蛋白和波形蛋白的免疫荧光染色。免疫荧光染色显示,敲除circKIF4A会增加上皮标记E-钙黏着蛋白的表达,同时会降低间质标记波形蛋白的表达。
K 建立了异种移植模型。L 肿瘤重量总结。为了进一步探索circKIF4A在体内的功能,建立了小鼠异种移植模型。circKIF4A的抑制作用显着降低了肿瘤的生长。
M 肺转移性结节的荧光素酶信号的代表性图像。N 肺转移性结节和HE染色切片的代表性图像。O 量化了转移性结节的数量。这表明circKIF4A的敲低抑制了TNBC中的细胞增殖和转移。** P <0.01
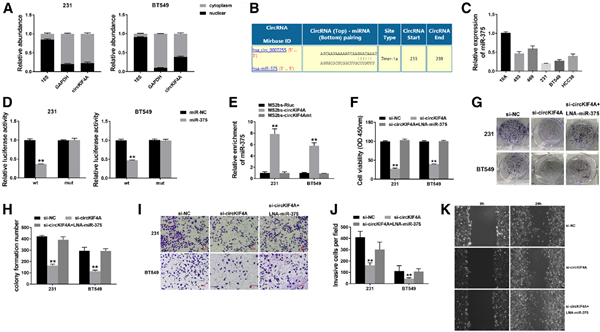
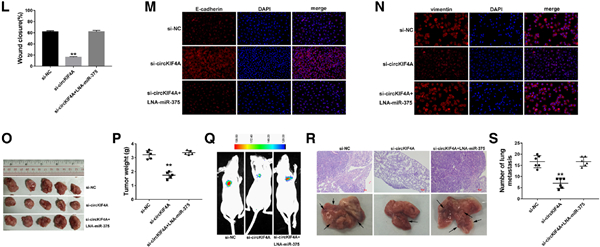
图3 circKIF4A充当miR-375a的海绵
A 检测到了核对照(18S),细胞质对照(GAPDH)和circKIF4A的表达水平。我们检测到circKIF4A在细胞内的位置,发现该circRNA主要位于细胞质中,这表明它可能起着miRNA海绵的作用。
B circKIF4A序列中miR-375的预测结合位点。我们使用环形RNA相互作用组预测了潜在的circRNA/miRNA相互作用。此外,在circKIF4A序列中发现了miR-375的结合位点。
C miR-375在TNBC细胞系中的表达。我们检测到miR-375在TNBC细胞系中的表达,并且miR-375被下调。
D 用miR-375模拟物和野生型或突变型荧光素酶报道基因共转染的细胞的荧光素酶测定。随后的萤光素酶报告基因检测表明,在野生型萤光素酶报告基因和miR-375模拟物共转染后,萤光素酶强度降低,而突变的萤光素酶报告基因没有这种作用。
E 用MS2bs-circKIF4A,MS2bs-circKIF4Amt或对照转染的基于MS2的RIP分析。为了确认circKIF4A和miR-375的直接结合,进行了RIP分析。 结果表明,miR-375主要集中在MS2bs-circKIF4A组中,这表明circKIF4A与miR-375直接相互作用,并可以充当miR-375的海绵。
F 用于检测细胞增殖的CCK-8分析。G 集落形成分析,以检测细胞集落形成能力。H 用Image J定量菌落形成数。为了确认circKIF4A和miR-375的直接结合,进行了RIP分析。 结果表明,miR-375主要集中在MS2bs-circKIF4A组中,这表明circKIF4A与miR-375直接相互作用,并可以充当miR-375的海绵。
I Transwell分析法评估细胞迁移能力。J 侵袭性的数量由Image J定量。K 用于检测细胞迁移能力的伤口愈合试验。L 伤口闭合由Image J量化。Transwell和伤口愈合试验显示,circKIF4A下调引起的细胞迁移能力下降,在miR-375抑制剂的作用下得以逆转。
M-N E-钙黏着蛋白和波形蛋白的m-n免疫荧光染色。免疫荧光染色显示,在miR-375抑制剂的作用下,circKIF4A敲除引起的E-cadherin和vimentin的表达改变被逆转。
O 建立异种移植模型。P 肿瘤重量总结。Q 肺转移性结节的荧光素酶信号的代表性图像。R 肺转移性结节和HE染色切片的代表性图像。 S 量化了转移性结节的数量。 ** P <0.01 M 在异种移植小鼠模型上进行的实验表明,使用miR-375抑制剂可以逆转circKIF4A抑制后肿瘤生长和肺转移的下降。所有这些结果表明circKIF4A通过海绵化miR-375在TNBC中发挥作用。
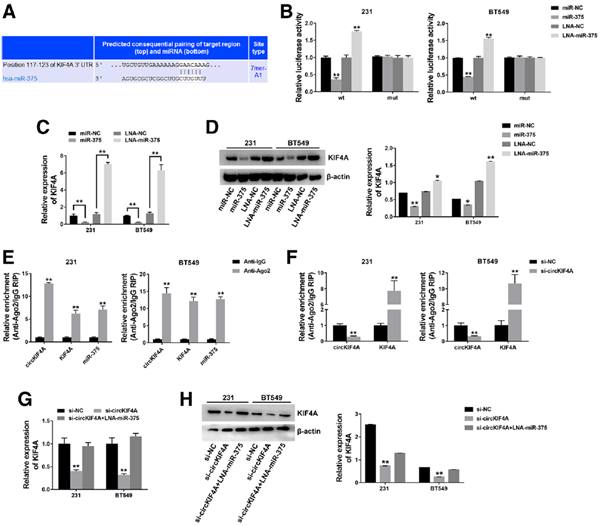
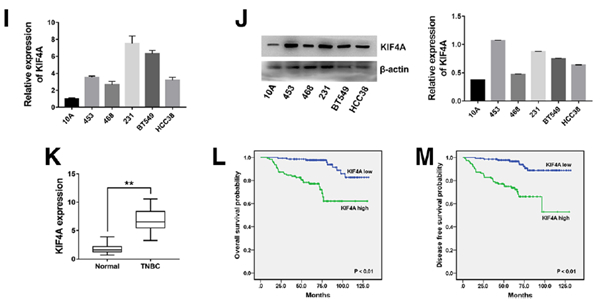
图4 circKIF4A充当ceRNA调节KIF4A
A KIF4A3’UTR中miR-375的预测结合位点。为了验证circKIF4A是否能分泌miR-375并释放其下游靶基因的表达,我们在TargetScan中搜索miR-375的潜在靶基因,并预测KIF4A。
B 转染细胞并进行荧光素酶测定。随后的荧光素酶报告基因实验显示,miR-375模拟物和野生型荧光素酶报告基因共转染后荧光素酶强度降低,而突变的荧光素酶报告基因则没有这种作用。转染野生型荧光素酶启动子和miR-375抑制剂后,荧光素酶强度升高。
C 转染细胞,并通过qRT-PCR检测KIF4A表达。D 通过以下方法检测到KIF4A表达免疫印迹(左)和定量(右)。此外,miR-375可以抑制KIF4A的表达,而miR-375抑制剂可以增加KIF4A的表达。此外,miR-375可以抑制KIF4A的表达,而miR-375抑制剂可以增加KIF4A的表达(图4c和d),这表明KIF4A可能受到miR-375的调控。
E RIP分析显示circKIF4A,KIF4A和miR-375在Ago2上富集。在Ago2上进行的RIP分析表明,circKIF4A,KIF4A和miR-375主要富集到Ago2,这表明circKIF4A和KIF4A被募集到Ago2相关的RISC中,它们与miR-375相互作用。
F 转染细胞,并在Ago2上进行RIP分析。敲除circKIF4A会降低Ago2对circKIF4A的富集,而会增加Ago2对KIF4A的富集。
G 细胞被转染并通过qRT-PCR检测KIF4A表达。H 通过免疫印迹检测KIF4A表达(左)并定量(右)。circKIF4A可以充当ceRNA,并与KIF4A竞争以结合miRNA。 此外,circKIF4A敲低导致KIF4A表达下降,而用miR-375抑制剂转染可逆转这种下降。这说明circKIF4A通过海绵体内的miR-375来调控KIF4A的表达。
I 通过qRT-PCR检测TNBC细胞系中KIF4A的表达。J 通过蛋白质印迹法(左)确定并定量(右)确定TNBC细胞系中KIF4A的表达。K KIF4A在57对TNBC组织和正常相邻组织中的表达。我们研究了KIF4A在TNBC细胞系和组织中的表达,发现KIF4A过表达。
L 240例TNBC患者的OS曲线。 240位TNBC患者的。M DFS曲线。我们调查了KIF4A对TNBC的临床影响,发现KIF4A与淋巴结转移和TNM分期呈正相关,这表明KIF4A在TNBC进程中起着至关重要的作用。 Kaplan-Meier生存分析还显示,KIF4A表达与TNBC较差的生存呈正相关。** P <0.01
创新点
已发现许多circRNA被解除调节并在各种癌症中充当致癌刺激物或肿瘤抑制物。 例如,已报道circFoxo3促进癌症中的细胞凋亡并抑制血管生成和细胞周期进程,而ciRS-7通过增强EGFR / RAF1 / MAPK途径来促进细胞周期进程。 在这里,我们重新分析了TNBC中circRNA的表达,发现circKIF4A显着上调,并与TNBC患者的肿瘤大小,淋巴结转移,TNM分期和较差的结果呈正相关。越来越多的证据表明,circRNA是重要的转录后调节因子。 由于它们所含的MRE丰富,稳定且具有潜在数量,circRNA是有效的miRNA海绵体。因此,circKIF4A可以作为TNBC的预后生物标志物和治疗靶标。
Abbkine专注于免疫学和细胞学领域,致力于创新和研发各类抗体、蛋白质、分析试剂与试剂盒,以期成为生命科学研究发展、药物研发等领域的关键推动者。在这里,我们为您呈献蛋白和免疫研究用户最喜爱的产品,从免疫学基础产品,如蛋白提取定量,到免疫学实验的内参标签抗体、一抗及二抗等;细胞研究用户最喜爱的产品,从用于检测细胞状态的染料及试剂盒,细胞器提取试剂盒,细胞亚结构染色示踪及细胞代谢检测产品,到用于细胞培养的细胞因子及蛋白类检测试剂盒,只为助力您的研究事业!
About Abbkine Scientific Co., Ltd.
Abbkine Scientific Co., Ltd.成立于2012年。我们的使命,通过为全球科学家提供人类和动物健康研究所需的基础研究工具,以期成为研究探索的关键推动者。我们将通过明确的核心战略和促进诚信、开放、合作、创新和为客户服务的企业文化,为全球生命科学研究者提供买得起的高品质产品,实现我们的使命。







