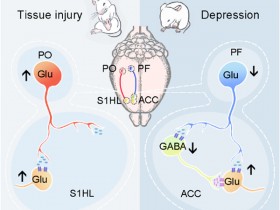
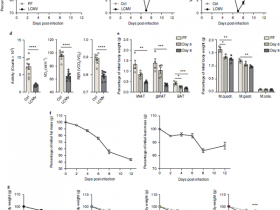
1.Nature:诱导CD8 T细胞的11株肠道菌,或能强化癌症治疗
IF:41.577
来自日本庆应义塾大学医学院的Kenya Honda博士带领团队发表研究,他们找到了11株肠道微生物,能够增加CD8+T细胞的水平,增强由它介导的抗肿瘤免疫反应,抑制肿瘤进展的效果与免疫检查点抑制剂持平,甚至更好!两者联合使用时,抗肿瘤效果更加优秀。
研究人员从健康人粪便中分离出11株细菌,研究人员还发现,这11株菌株组成了一个“联合体”(11-mix),它们共同发挥作用,其中,4株非拟杆菌目的细菌是联合体的“核心”(4-mix),另外7株拟杆菌目的细菌(7-mix)则扮演着“支持者”的角色。
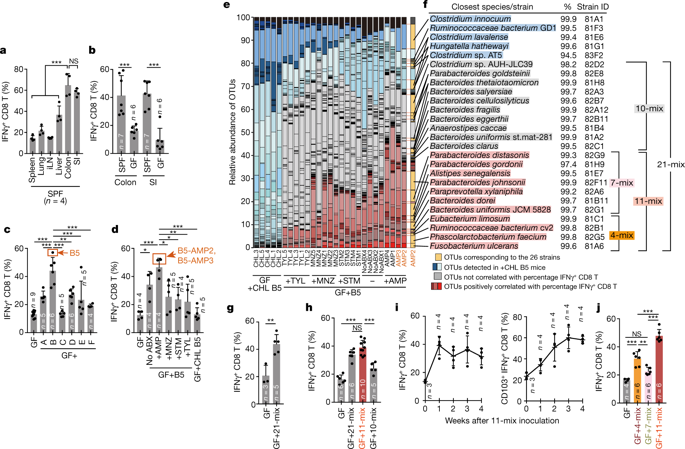
图片来源【Nature】
当联合定植于肠道时,可在小鼠肠道和其它器官中有效诱导能生成IFN-γ的CD8 T细胞,而不引起炎症;该诱导作用依赖于CD103+树突细胞和MHC Ia抗原呈递分子;共定植这11株菌不仅能提高小鼠对李斯特致病菌感染的抗性,还能增强IFN-γ+ CD8 T细胞介导的抗肿瘤免疫,抑制小鼠肿瘤进展,强化免疫检查点抑制剂的疗效而不引起结肠炎副作用;这11株菌在人肠道中普遍丰度低,有望用于治疗癌症和感染等疾病。
评论:总的来说,它仍然是一个“突破性”的进展,因为这是首次鉴定出的,一个可以增强免疫检查点抑制剂效果的人类肠道细菌“联合体”,它们为利用肠道微生物治疗癌症这个愿景提供了又一条可行的通路。
原始出处:Takeshi Tanoue, Satoru Morita, Damian R. Plichta, et al.A defined commensal consortium elicits CD8 T cells and anti-cancer immunity. Nature. 23 January 2019
2. Science:动脉粥样硬化发生机制研究领域重要进展
IF: 41.058
中南大学湘雅医院老年病科柏勇平副教授课题组与美国德州医学中心Longhou Fang副教授团队合作,在动脉粥样硬化发生机制研究领域取得重要进展。该成果系统地阐述了高脂血症与造血过程关联的具体分子机制,并揭示了AIBP通过上述两个通路对于生血内皮造血过程的调控作用及在动脉粥样硬化疾病中的具体影响。
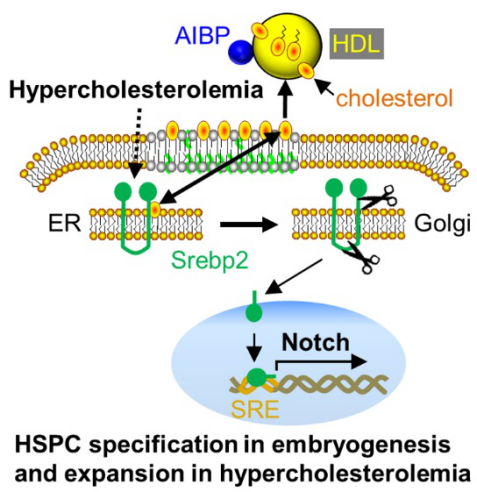
高胆固醇血症是动脉粥样硬化发生、发展的重要驱动因素,并促进了动脉粥样硬化过程中造血干祖细胞(HSPC)的扩增,然而,高胆固醇血症与机体造血功能之间的联系因素及机制不明。该研究首先观察到血浆胆固醇水平增高能激活内皮细胞SREBP2,并与Notch1信号通路共同作用激活生血内皮,从而促进HSPC的增殖和动员及炎症因子的释放,推动了动脉粥样硬化的发生进程。随后该研究通过多种技术方法确定了一种特殊载脂蛋白结合蛋白AIBP在SREBP2和Notch1信号通路之间发挥的关键调控作用。
评论:该研究为临床动脉粥样硬化疾病的防治提供了新的切入点。
原始出处:
Qilin Gu,et al.AIBP-mediated cholesterol efflux instructs hematopoietic stem and progenitor cell fate.Science.31 Jan 2019:eaav1749
3. Curr Biol:新技术有望大幅提高试管婴儿的成功率
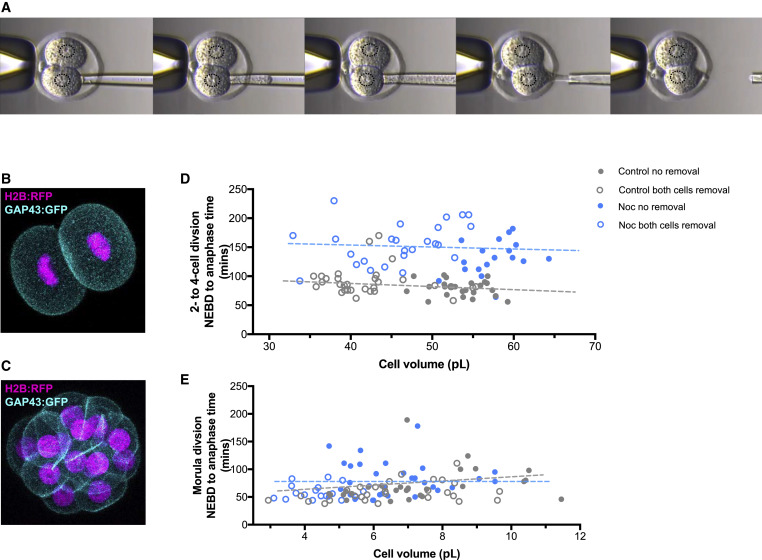
在体外受精过程中所产生的胚胎中,大约一半胚胎都含有染色体数目异常的细胞,这种异常称之为非整倍性,其在生殖生物学中是众所周知的,并被认为是引起不孕不育的一个主要原因。研究者Greg FitzHarris说道,这项研究中我们至少解释了其中一个原因,即为何体外受精技术所得到的胚胎为何会携带染色体数目异常的细胞。如果利用简单药物对小鼠胚胎的检查点进行操控,研究者就能够将胚胎发生错误的几率降低一半。
通过加入合适剂量的合成物质proTAME,研究者就观察到,每个小鼠胚胎中有大比例的细胞都会拥有正常数量的染色体;在小鼠机体中,一个正常的卵母细胞含有20对染色体,而人类则拥有23对染色体。但提及体外受精技术,制成最佳的胚胎或许是成功的关键。目前这一研究仍处于基础研究阶段,而且仅在实验室的小鼠机体中进行了试验,研究者强调,当在人类机体中进行应用时一定要非常谨慎。
来自蒙特利尔大学医学研究中心的科学家们通过研究在实验室中成功减少了小鼠胚胎缺陷的数量,这一研究发现有望转化到人类研究中,提高不孕不育夫妇生育的机会。刊登在国际杂志Current Biology上。
评论:望这新技术可以制造出更好的胚胎,大幅提高试管婴儿的成功率。
原始出处:
Cayetana Vázquez-Diez,Lia Mara Gomes Paim,Greg FitzHarris,et al. Cell-Size-Independent Spindle Checkpoint Failure Underlies Chromosome Segregation Error in Mouse Embryos, Current Biology, February 14, 2019,doi:10.1016/j.cub.2018.12.042