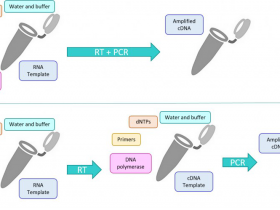
逆转录PCR(reverse transcription PCR)或者称反转录PCR(reverse transcription-PCR, RT-PCR),是聚合酶链式反应(PCR)的一种广泛应用的变形。它是一种以 RNA 为样本,RNA链被逆转录成为互补DNA(cDNA),再以此为模板通过 PCR 进行 DNA 扩增。
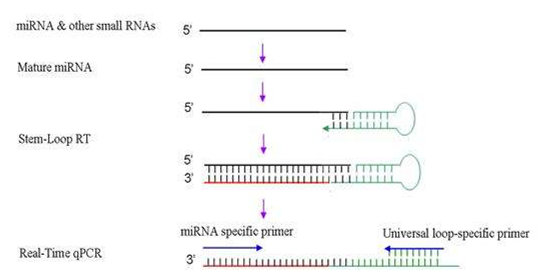
图源:百度百科
一、RT-PCR的指数扩增
RT-PCR的指数扩增是一种很灵敏的技术,可以检测很低拷贝数的RNA。RT-PCR广泛应用于遗传病的诊断,并且可以用于定量监测某种RNA的含量。
RT-PCR的关键步骤是在RNA的反转录,要求RNA模版为完整的且不含DNA、蛋白质等杂质。在完成逆转录过程之后,通过PCR进行定量分析的时候,随着技术的发展,real-time PCR(实时荧光PCR)或ddPCR(数字PCR)技术也被用来做定量分析,它们比普通PCR进行定量分析时灵敏度更高,定量更精确。
二、PCR引物的选择
对靶序列中潜在的引物位点进行分析, 这些位点应该不会形成同源多聚体结构,也没有明显的形成二级结构的趋势,不会自身互补,与基因组中的其他序列无显著的同源性。
(1)依据寡核苷酸引物与其靶序列形成杂合分子的熔解度的计算中提供的公式计算各引物的熔解温度。
(2)选择一对匹配完好的正向和反向引物。两条引物的G+C含量相似,将产生一种大小和碱基组成合适的产物。两条引物与所扩增片段的GC含量都应在40%-60%之间。
(3)对寡核苷酸的长度和/或位置进行细调。使得引物的3‘末端核苷酸为G或C。检查两条寡核苷酸之间有无明显的互补性。作为一条经验性的规律,一条引物上不该含有三个连续的与另一条引物互补的核苷酸。
三、注意事项
图源:百度百科
(1)双链DNA的变性温度是由双链中C+G的含量决定的,C+G含量越高,模板DNA的溶解温度就越高。在选择的变性温度下,模板链越长变性所需时间就越长。如果变性温度过低或变性时间过短,会使仅仅富含A+T区域变性。当模板DNA的G+C含量超过55%的时需要更高的变性温度。
(2)复性过程采用的温度至关重要如果复性温度太高,寡核苷酸引物不能与模板很好的复性,扩增效率将会降低。如果复性温度太低,引物将产生非特异性复性,从而导致非特异性的DNA片段的扩增。复性通常在比理论计算的引物和模板的溶解温度低3—5℃的条件下进行。
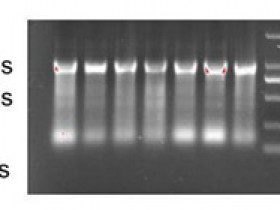
(3)PCR扩增所需的循环数目决定于反应体系中起始的模板拷贝数以及引物延伸和扩增的效率。一旦PCR反应进入几何级数的增长期,反应会一直持续下去,直至某一成分成为限制因素。从这一点上来说,扩增产物中绝大多数应该是特异性的扩增产物,而非特异性的扩增产物应该低到难以检测到的程度。用TaqDNA聚合酶(效率为0.7)在一个含有10的5次方个拷贝的靶序列的反应体系中进行30个循环后往往可以做到上述的理想情况。