已有的研究显示,环境因素可以深刻地影响多细胞生物体中的细胞可塑性。例如,运动可以促进骨骼肌中的糖酵解-氧化纤维型转换,并且冷驯化可以诱导脂肪组织中的米色脂肪细胞的生物发生。然而,至今为止,我们对于生理或病理线索引起发育可塑性的分子机制仍未完全了解。
最近,研究人员报导了一种米色脂肪细胞,在缺乏β-肾上腺素能受体信号传导的情况下,该细胞在慢性冷适应中起关键作用。就发育起源和调节而言,该米色脂肪与常规米色脂肪不同,其显示出增强的葡萄糖氧化。因此,研究人员将其称为糖酵解米色脂肪。
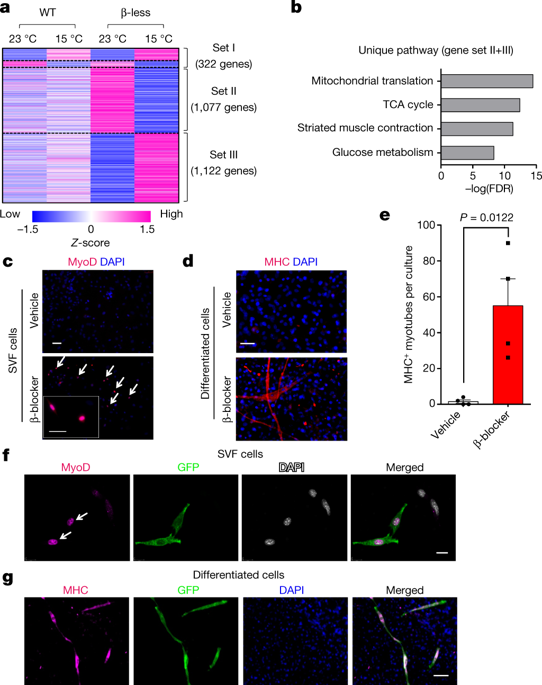
在机理上,研究人员通过肌源性中间体鉴定GA结合蛋白α作为糖酵解米色脂肪细胞分化的调节剂。
因此,以上研究揭示了一种非传统的适应性机制,通过该机制,热应激诱导祖细胞可塑性,并募集能量稳态和存活所需的不同形式的产热细胞。
参考资料:
Chen Y et al. Thermal stress induces glycolytic beige fat formation via a myogenic state. NATURE 2018, DOI: 10.1038/s41586-018-0801-z.
由肿瘤特异性的蛋白编码突变产生的新抗原(neoantigen)不会产生中枢耐受性,能够产生强效的免疫反应并且能够作为促进肿瘤排斥的真正抗原发挥作用。在一项新的I/Ib期临床试验中,来自美国布莱根妇女医院、哈佛医学院、达纳-法伯癌症研究所和布罗德研究所的研究人员证实一种多表位的个人化新抗原疫苗接种策略对通常具有相对较低的突变负荷和免疫“冷”肿瘤微环境的胶质母细胞瘤等肿瘤是可行的。
这种疫苗接种策略之前已在高风险黑色素瘤患者中测试过。相关研究结果于2018年12月19日在线发表在Nature期刊上,论文标题为“Neoantigen vaccine generates intratumoral T cell responses in phase Ib glioblastoma trial”。
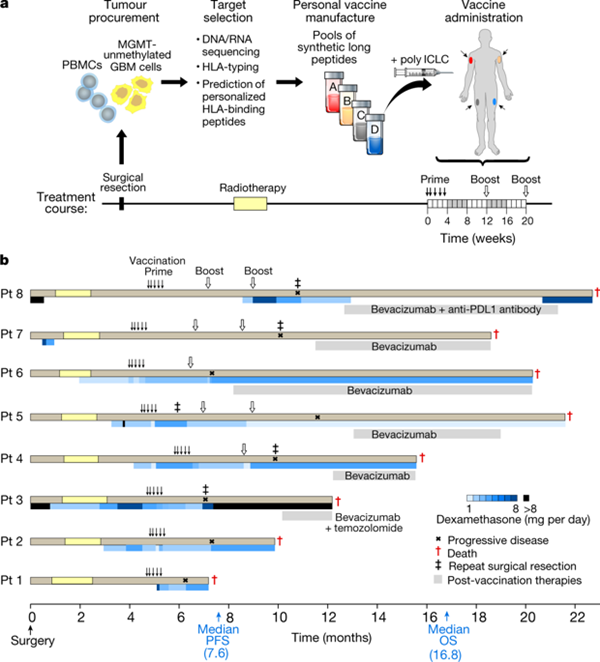
图片来自Nature
在这项I/Ib期临床试验中,这些研究人员利用个人化的新抗原靶向疫苗让接受手术切除和常规放疗后新诊断为胶质母细胞瘤的患者进行免疫接种。未接受地塞米松(dexamethasone)治疗的患者产生循环多功能性的新抗原特异性的CD4+ T细胞和CD8+ T细胞反应,而且这些反应富集于一种记忆表型中,并表现出肿瘤浸润性T细胞数量上的增加,其中地塞米松是一种高效的皮质类固醇,经常用于治疗胶质母细胞瘤患者的脑水肿。
通过使用单细胞T细胞受体分析,他们提供证据表明来自外周血的新抗原特异性T细胞能够迁移到颅内胶质母细胞瘤肿瘤中。综上所述,这种新抗原靶向疫苗有潜力有利地改变胶质母细胞瘤的免疫环境。
参考资料:
Derin B. Keskin et al. Neoantigen vaccine generates intratumoral T cell responses in phase Ib glioblastoma trial. Nature, 2018, doi:10.1038/s41586-018-0792-9.
3、针对新诊断的胶质母细胞瘤进行积极个性化的疫苗接种试验
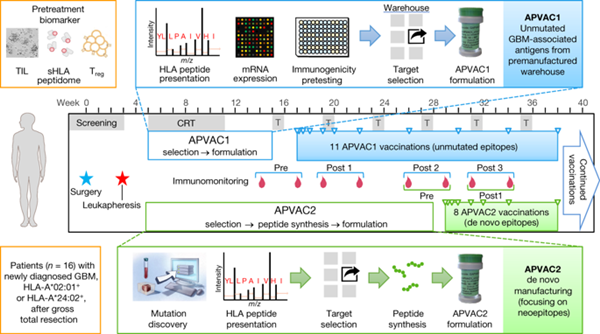
目前,胶质母细胞瘤患者尚未充分受益于最近大热的检查点抑制剂等癌症治疗方面的突破。对于使用检查点抑制剂成功的治疗,高突变负荷和对新表位的反应被认为是必不可少的。胶质母细胞瘤中免疫细胞的肿瘤内浸润有限,这些肿瘤仅含有30-50个非同义突变。利用肿瘤抗原的完整全集 - 即未突变的抗原和新表位 - 可以提供更有效的免疫疗法,尤其是对于具有低突变负荷的肿瘤。
最近,在胶质瘤主动个性化疫苗联盟(GAPVAC)的I期试验GAPVAC-101中,研究人员将高度个性化的疫苗接种与两种类型的肿瘤抗原整合到标准治疗中,以最佳地利用新诊断的胶质母细胞瘤患者的有限目标空间。
15例患有人白细胞抗原(HLA)-A * 02:01或HLA-A * 24:02阳性的胶质母细胞瘤患者用来自预制的未突变抗原文库的疫苗(APVAC1)进行治疗,然后用APVAC2治疗,优先治疗有针对性的新表位。个性化基于个体肿瘤的转录组和免疫肽的突变和分析。
GAPVAC方法是可行的,并且具有聚-ICLC(多核糖核苷 - 多聚胞苷酸 - 聚-L-赖氨酸羧甲基纤维素)和粒细胞-巨噬细胞集落刺激因子作为佐剂的疫苗显示出有利的安全性和强免疫原性。未突变的APVAC1抗原引发中枢记忆CD8+ T细胞的持续反应。APVAC2主要诱导T辅助细胞1型对抗预测的新表位的CD4+ T细胞应答。
参考资料:
Hilf N et al. Actively personalized vaccination trial for newly diagnosed glioblastoma. NATURE 2018, DOI: 10.1038/s41586-018-0810-y.