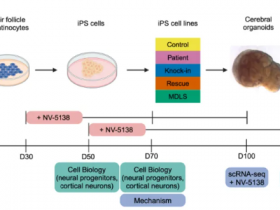
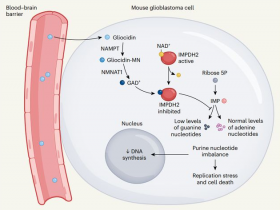
2024年11月6日,来自美国纽约大学格罗斯曼医学院Abhishek Bhardwaj团队在《自然》杂志上发表了标题为“A mechanism for hypoxia-induced inflammatory cell death in cancer.”的重要工作进展,研究提出了癌症中缺氧诱导炎症细胞死亡的机制,低氧如何通过一种独特的机制诱导癌细胞死亡。这项研究探讨了蛋白酪氨酸磷酸酶(PTP1B)与RNF213蛋白的相互作用如何在低氧情况下诱导乳腺癌细胞死亡,为针对低氧肿瘤的治疗提供了新思路。

据介绍,缺氧癌症细胞抵抗许多抗肿瘤治疗,并可能导致复发。肿瘤微环境通常具有低氧或缺氧区域,癌细胞可以通过激活多种信号通路来适应这一环境。在正常氧气水平下,低氧诱导因子(HIF1α和HIF2α)会被羟基化,并最终降解。然而,在低氧环境中,HIF因其因子稳定,进一步激活NF-κB等多种存活相关基因的表达。PTP1B位于内质网中,并参与胰岛素与瘦素等信号的调控,此前研究表明,其在低氧环境下能够通过RNF213调节癌细胞的生死。
研究人员之前发现蛋白酪氨酸磷酸酶(PTP1B)的缺乏或抑制通过激活RNF213(一种具有多个AAA-ATPase结构域和两个泛素连接酶结构域(RING和RZ)的大蛋白)促进人表皮生长因子受体2阳性乳腺癌症细胞在缺氧时死亡,RNF213与烟雾病、脂毒性和先天免疫有关。
研究人员发现,PTP1B和ABL1/2相互控制RNF213酪氨酸磷酸化,从而控制其寡聚化和RZ结构域激活。RZ结构域普遍存在并诱导NF-κB主要调节因子CYLD/SPATA2的降解。CYLD/SPATA2水平的降低导致NF-κB活化和NLRP3炎性小体的诱导,再加上缺氧诱导的内质网应激,引发焦亡细胞死亡。与该模型一致,CYLD缺失表型,而NLRP3缺失阻断PTP1B缺乏对人表皮生长因子受体2阳性乳腺癌症异种移植物生长的影响。对RNF213突变体的重组研究证实,RZ结构域介导肿瘤细胞死亡。
总之,这一研究结果确定了一种独特的、潜在可靶向的PTP1B-RNF213-CYLD-SPATA2通路,该通路对控制缺氧性肿瘤中的炎性细胞死亡至关重要,为RNF213调控提供了新的见解,并对烟雾病、炎性疾病和自身免疫性疾病的发病机制具有潜在意义。
文章来源:
Bhardwaj, Abhishek, Panepinto, Maria C. et al, A mechanism for hypoxia-induced inflammatory cell death in cancer.DOI: 10.1038/s41586-024-08136-y,Nature:最新IF:69.504