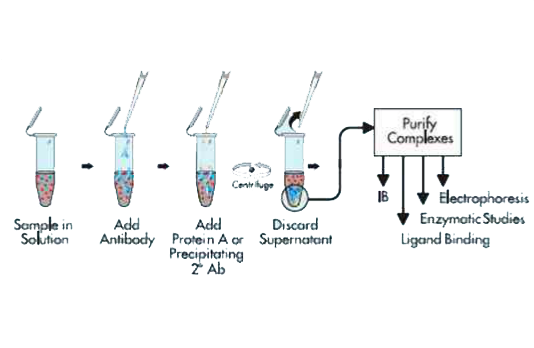
免疫沉淀(IP)是利用抗原蛋白质和抗体的特异性结合以及细菌蛋白质的“Protein A/G”特异性地结合到抗体(免疫球蛋白)的Fc片段的现象开发出来的方法。目前多用protein A/G预先结合在argarose beads上,使之与含有抗原的溶液及抗体反应后,beads上的protein A/G就能达到吸附抗原的目的,通过低速离心,可以从含有目的抗原的溶液中将目的抗原与其它抗原分离。
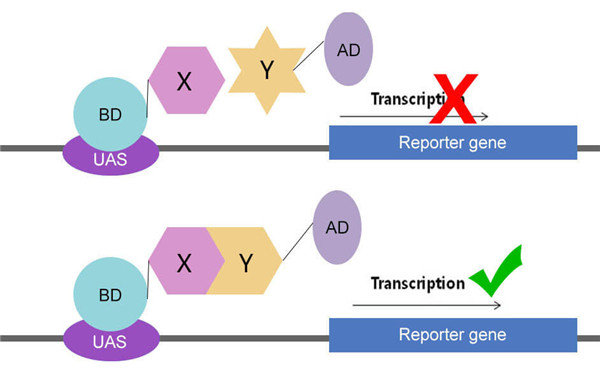
免疫共沉淀(Co-IP)是以抗体和抗原之间的专一性作用为基础的用于研究蛋白质相互作用的经典方法,是确定两种蛋白质是否在生理条件下有相互作用的有效方法。其原理是:当细胞在非变性条件下被裂解时,完整细胞内存在的许多蛋白质-蛋白质间的相互作用被保留了下来。如果用蛋白质X的抗体免疫沉淀X,那么与X在体内结合的蛋白质Y也能沉淀下来。这种方法常用于测定两种目标蛋白质是否在体内结合;也可用于确定一种特定蛋白质的新的作用蛋白。
染色质免疫沉淀(ChIP)是研究体内DNA与蛋白质相互作用的重要工具。它的基本原理是在生理状态下把细胞内的蛋白质和DNA交联在一起,超声波将其打碎为一定长度范围内的染色质小片段,然后通过所要研究的目的蛋白质特异性抗体沉淀此复合物,特异性地富集目的蛋白结合的DNA片段,通过对目的片段进行PCR检测,可以知道目的蛋白与哪些基因作用。
在实验操作中所要注意的关键点
免疫沉淀:因为免疫沉淀的目的主要是通过抗体和目的蛋白相互作用从而捕获目的蛋白,所以实验中要注意的关键点是抗体和目的蛋白相互作用的效果。其主要受抗体的结合能力,目的蛋白和抗体的可接触性两个因素影响。所以免疫沉淀实验中的关键因素是抗体的选择以及裂解缓冲液中的配方。对于前者而言,抗体所针对的作用表位必须处于目的蛋白表面,对抗体结合力的要求和免疫印迹或者免疫荧光相比要高得多;对于后者而言,主要考虑因素是缓冲液中的去垢剂成分能否在不破坏目的蛋白天然构像的情况下(不影响目的蛋白和抗体的相互作用效果)将目的蛋白从细胞局部定位(比如位于某些细胞器中)中有效释放出来。
免疫共沉淀:免疫共沉淀的目的是通过抗体和目的蛋白的相互作用从而捕获目的蛋白复合物,最终检测目的蛋白复合物中各成分之间的相互作用,所以实验中要注意的关键点和免疫沉淀相比,除了要注意抗体和目的蛋白相互作用的效果外,还要注意目的蛋白复合物的完整性,后者主要考虑因素是缓冲液中的去垢剂成分能否在有效释放目的蛋白复合物进入可溶相的情况下不破坏目的蛋白复合物中各成分之间的相互作用。所以,免疫共沉淀实验中的关键因素除了抗体的选择外,裂解缓冲液配方中的去垢剂的成分和浓度对免疫共沉淀实验的成功与否至关重要,其选择相比免疫沉淀实验而言,要求更严格。
染色质免疫共沉淀:染色质免疫共沉淀的主要目的是通过抗体和目的蛋白的相互作用从而捕获和目的蛋白有相互作用的DNA片段,最终检测目的蛋白和DNA片段的相互作用。因此,实验中要注意的关键点和前二者(免疫沉淀和免疫共沉淀)有所不同。因为在实验中蛋白质-DNA复合物的维持需要依靠多聚甲醛的交联作用,所以目的蛋白的许多表面表位也在交联过程中丧失。因此,除了后续的基本操作和免疫沉淀以及免疫共沉淀有些许不同,有额外需要注意的是,其对抗体的要求要比免疫沉淀和免疫共沉淀高得多,相对而言,裂解缓冲液的成分并不是关键因素。
我们该选择什么样的抗体?
在所有免疫沉淀相关实验中,抗原的起始浓度相对其它免疫相关实验(WB和IF等)要低得多,所以对抗体的亲和力相对其它实验提出了更高的要求,这就需要使用高亲和力的抗体去进行免疫沉淀相关实验。同时,由于免疫沉淀相关实验主要是在生理条件下进行,所以需要抗体识别蛋白的天然表面构像,因此选择的抗体其针对的抗原决定簇需要暴露在蛋白表面。这些因素对制备能成功应用于IP实验的抗体提出了很高的要求:
1、用于免疫的蛋白抗原,其构像需要尽量接近目的蛋白的天然构像或者用于免疫的多肽尽量暴露在目的蛋白的表面。获得接近天然构像的蛋白抗原的途径有很多,主要有天然提取,原核表达重组蛋白以及真核表达重组蛋白三种方式。这其中,就蛋白构像角度而言,天然提取是最佳途径,但这种方法受材料来源限制和纯化方法复杂等多因素影响,一般很少采用。原核表达因为成本低廉,操作方便,最为受欢迎,但其受表达环境与大部分蛋白天然存在环境差别巨大,构像失真情况严重,抗原的构像质量有严重问题。大规模瞬时真核表达是近期新兴的表达系统,具有表达环境接近天然,操作方便等诸多优点,是获取具有天然构像蛋白抗原的首选工具。
2、亲和力要比普通的抗体应用要求高得多。多克隆抗体由于可以结合目的抗原的多个抗原决定簇,所以在亲和力方面是首选。但考虑到特异性,获得单克隆抗体群是更好的选择。具体优缺点总结如下表。
| 多克隆抗体 | 单克隆抗体 | 单克隆抗体群(由一个免疫原产生的多个单克隆抗体混合物) | |
| 抗体抗原作用信号强度 | 极佳 | 由抗体的亲和力决定(极佳或者极弱) | 极佳 |
| 特异性 | 通常很好,但有时会有非特异性相互作用 | 极佳,但有时会有交叉反应 | 极佳(由于选择可以进行IP且没有交叉反应的抗体 组成单克隆抗体群) |
| 优点 | 亲和力高(由于抗体可以与目的蛋白的多个抗原决定簇相互作用) | 特异性好,且可以无限量供应 | 特异性好,亲和力高 |
| 缺点 | 非特异性相互作用很难去除 | 需要筛选亲和力高的抗体,抗原表位可能会被相互作用蛋白遮蔽 | 能够筛选得到的符合条件的单克隆并不多,所以单克隆抗体群也就不容易获得 |
| 免疫沉淀效果 | 极佳 | 由抗体的亲和力决定 | 极佳 |
| 免疫共沉淀效果 | 通常很好,但有时非特异性相互作用会带来假阳性 | 由抗体的亲和力决定和抗原表位是否被相互作用蛋白遮蔽决定(极佳或极弱) | 极佳 |
| 染色质免疫沉淀效果 | 通常很好,但有时非特异性相互作用会带来假阳性 | 由抗体的亲和力决定和抗原表位是否被遮蔽或者抗原表位是否被交联实验所破坏 | 极佳 |
疑难问题
1、免疫沉淀
| 产生的问题 | 产生问题的原因 | 解决办法 |
|
没有得到目的蛋白或者得到的目的蛋白太少
|
目的蛋白在样品中含量太低或者检测样品中没有目的蛋白 | 更换样品或者在细胞中过表达目的基因 |
| 加入的protein A/G-beads太少或者与一抗的结合属性不匹配 | 增加protein A/G-beads至60ul/mg总蛋白;检查protein A/G-beads与一抗的结合属性 | |
| 抗体或者protein A/G-beads与样品作用时间太短 | 正确按照protocol操作,抗体或者protein A/G-beads与样品作用时间最短不能少于2h | |
| 蛋白发生降解 | 尽量使用新鲜制备样品进行免疫沉淀实验;将样品至于冰上或者在冷库中操作 | |
| 杂蛋白太多 | 加入抗体和protein A/G-beads前100000g离心细胞30min以去除膜成分或者不可溶蛋白 | |
| 目的蛋白没有溶解或者溶解不充分 | 针对目的蛋白的特性选择合适的裂解液 | |
| 抗体使用浓度太低 | 提高抗体使用浓度 | |
| 抗体亲和力差 | 更换亲和力更高的抗体 | |
| 抗体所识别的抗原表位被相互作用蛋白所遮蔽,无法与目的蛋白相互作用 | 更换抗体 | |
| 抗体选择不合适,所选抗体不能识别处于天然构象的蛋白 | 更换抗体 | |
| 洗涤条件过于剧烈 | 减少洗涤次数,降低洗涤缓冲液中的盐浓度或者更换更温和的去垢剂 | |
| 检测灵敏度不够 | 更换检测试剂(针对WB检测)或者提高检测水平(针对质谱检测) | |
|
有非特异性相互作用或者严重的交叉反应
|
Protein A/G-beads对蛋白的非特异性吸附或者样品中有其他蛋白与protein A/G-beads有交叉反应 | 用protein A/G-beads对细胞进行预处理去除非特异性吸附蛋白,然后再加入抗体;加入2% BSA于protein A/G-beads中对beads进行预封闭 |
| 抗体特异性不好 | 更换抗体或者设立阴性对照(IgG或者其它无关抗体) | |
| 裂解液配方过于温和 | 使用条件更加剧烈的裂解液配方(比如RIPA缓冲液) | |
| 洗脱条件过于温和 | 使用高盐(大于150nM NaCl)或者其它强表面活性剂洗脱 | |
| 目的蛋白大小与IgG的重链和轻链接近 | 使用不同种属的抗体分别进行IP和WB实验 | |
| 使用交联剂DSS将一抗与protein A/G-beads共价偶联后进行免疫沉淀实验 |
2、免疫共沉淀
| 产生的问题 | 产生问题的原因 | 解决办法 |
|
没有检测到与目的蛋白相互作用的蛋白或者检测得到的信号太弱 |
裂解液中的去垢剂浓度过高或者配方过于剧烈 | 降低去垢剂浓度或者更换去垢剂种类(按作用剧烈程度来区分:SDS>Trition>NP40>Digitonin>CHAPS) |
| 受蛋白的亚细胞定位影响 | 重新选择裂解液配方以释放目的蛋白 | |
| 蛋白与蛋白之间的相互作用太弱或者不太稳定 | 选择亲和力更高的抗体以捕获更多的目的蛋白从而捕获更多的相互作用蛋白;过表达提高目的蛋白的含量;选择目的蛋白或者相互作用蛋白含量高的样品进行免疫共沉淀实验 | |
| 假阳性太大,有太多非特异性相互作用蛋白被检测到 | 抗体浓度过高 | 降低抗体作用浓度 |
| 抗体特异性不好 | 更换抗体 |
3、染色质免疫沉淀
| 产生的问题 | 产生问题的原因 | 解决办法 | 备注 |
|
没有检测到与目的蛋白相互作用的DNA片段或者检测到的信号太弱
|
染色体片段太小 | 超声(X-CHIP)或酶解(N-CHIP)片段不要小于500bp | |
| 过度交联 | 严格按照protocol进行操作,多聚甲醛交联时间控制在10-15min | 多度交联会导致更多的抗原表位被破坏,影响抗体与目的蛋白的结合 | |
| 用于实验的染色体量不够 | 不要少于25ug | ||
| 使用N-CHIP方法去进行实验 | 当目的蛋白和DNA片段之间的相互作用比较弱时改用X-CHIP方法 | 组蛋白与DNA片段之间的作用比较强,可以使用N-CHIP方法 | |
| 使用了不合适的单抗 | 使用多抗或者单克隆抗体群或者更换合适的单抗 | 多聚甲醛交联会破坏许多抗原表位使得某些单抗的作用效果减弱 | |
| 目的蛋白没有与待测DNA片段结合 | 使用阳性对照判断CHIP实验是否成功 | ||
| PCR实验失败(引物设计不合理或者PCR反应条件不佳) | 重新设计引物或者摸索最佳PCR条件 | ||
| 假阳性太大,有太多非特异性结合DNA片段被检测到 | 抗体浓度过高 | 降低抗体作用浓度 | |
| 抗体特异性不好 | 更换抗体 | ||
| PCR污染 | 重新配制PCR缓冲液 |