2024年2月19日,来自北京大学Li Qiang和Liheng Wang小组合作在国际学术期刊《细胞-代谢》发表了标题为“IgG is an aging factor that drives adipose tissue fibrosis and metabolic decline.”的研究成果。他们的研究表明IgG是促使脂肪组织纤维化和代谢减慢的衰老因子。
据介绍,衰老具有明显的新陈代谢减弱;然而,衰老的诱导因素仍有待阐明。
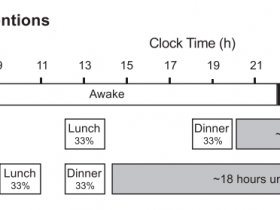
研究人员发现IgG在衰老过程中会发生积累,尤其是在白色脂肪组织(WAT)中,这会损害脂肪组织的功能和代谢健康。热量限制(CR)会减少IgG在白脂肪组织中的积累,而补充IgG则会抵消CR带来的代谢益处。IgG通过Ras信号激活巨噬细胞,进而利用TGF-β/SMAD途径诱导脂肪组织纤维化。
研究团队设计了一种靶向IgG循环调节受体FcRn的反义寡核苷酸(ASO)来纠正衰老过程中IgG的积累,结果显示,ASO治疗显著降低血浆、WAT、BAT和肝脏中的IgG水平。因此,靶向IgG的循环调节受体FcRn可以恢复衰老过程中的代谢功能。
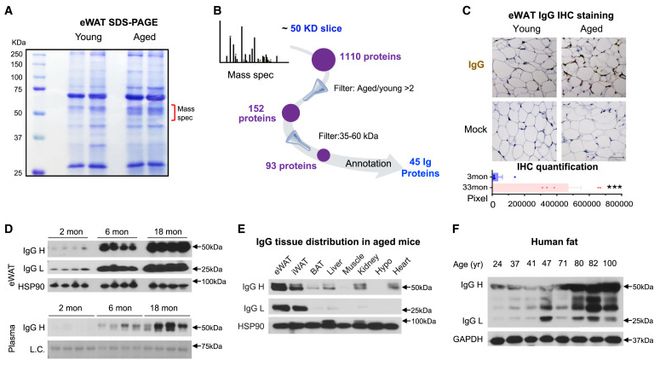
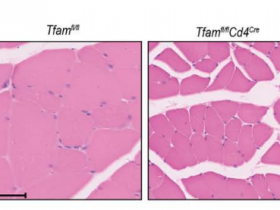
与此一致,除非暴露于IgG,否则缺乏B细胞的小鼠不会出现与衰老相关的WAT纤维化、炎症和胰岛素抵抗。条件性敲除巨噬细胞中的IgG循环受体-新生儿Fc受体(FcRn)-可防止衰老过程中IgG的累积,从而延长健康和寿命。
此外,通过反义寡核苷酸靶向FcRn能恢复老龄小鼠体内WAT的完整性和代谢健康。这些发现表明IgG是造成衰老的隐性罪魁祸首,并提出了一种恢复代谢健康的新策略。
文章来源:
Lexiang Yu, Qianfen Wan, Qiongming Liu et al,IgG is an aging factor that drives adipose tissue fibrosis and metabolic decline.