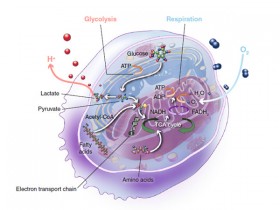
以前我们已经提到:表观遗传学已成为生命科学界最热门领域之一。以DNA为载体的中心法则仍是传递遗传信息的主要方式;而表观遗传可作为它重要的有益补充,而非你死我活的针锋相对。最近高通量测序的应用使表观遗传研究如虎添翼,新兴技术的出现,在细胞内新陈代谢和DNA表观遗传修饰间架起了一道桥梁,也为研究者对细胞生理功能的研究拓展了新的道路。
研究者现在已经知道细胞代谢过程中的某些因素是可以影响表观遗传效应的,新陈代谢的产物本身对细胞中一些基因的打开或关闭是有影响的。比如在糖或蛋白质代谢过程中所形成的分解产物,就可以对DNA或组蛋白进行表观遗传修饰。而且正常细胞和癌细胞也会以不同的方式进行代谢活动,并以不同的代谢物来进行遗传物质的表观遗传修饰。
因而了解细胞内哪些代谢物可以调控基因功能,以及它们是通过表观遗传手段,还是与转录因子或其他途径的结合来调控控基因功能对开发更好的药物至关重要。下面我们简单介绍几个利用高通量表观遗传技术来分析胞内代谢产物对细胞生理功能影响的案例。首先来看看目前最火的癌症领域:
一、癌症生物化学方面
研究项目:胰腺导管腺癌(胰腺癌的最常见形式)中的原发性肿瘤和转移性细胞在遗传上是彼此相似的。但转移性肿瘤细胞总会生长在比原发肿瘤更丰富的营养环境中,并以明显不同的方式生长。
虽然目前调控肿瘤细胞转移性扩散和生长的基因仍不清楚,但转移性癌细胞基因组中所存在明显的去甲基化现象,也表明表观遗传机制在起作用。Vanderbilt大学病理学家Oliver McDonald的研究小组则认为这种表观遗传变化可能会受到代谢变化的调控作用。
研究成果:当研究者将原发性和转移性人类肿瘤的配对样本与甲基化组蛋白进行比较时,他们发现来自远处部位(如肝脏和肺部)的转移细胞在其组蛋白上携带不同的甲基化和乙酰化标记。
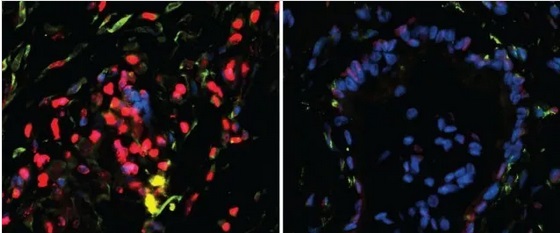
图中,首先形成胰腺瘤的细胞(左图)显示高水平的组蛋白甲基化(红色);而进行远处(如肝脏)转移的癌细胞中,甲基化现象已经完全丢失(右图)
与原发性肿瘤细胞不同,转移性癌细胞并没有利用其它“能源”来补充或代替葡萄糖,而是严重依赖葡萄糖消耗形成新肿瘤块。因此,研究人员使用液相色谱和高分辨率质谱来追踪肿瘤细胞转移后的糖代谢途径,并找到了癌细胞在这些途径中可能最依赖的步骤。
研究者在研究肿瘤的代谢物谱时发现,转移性癌细胞内的一种葡萄糖代谢产物6-磷酸葡萄糖酸(6PG)含量极低。而6PG可被6-磷酸葡萄糖酸脱氢酶(PGD)分解消耗,表明此酶过度活跃并消耗了所有的底物。
而敲除PGD基因并没有改变同一途径中其他酶的表达,却逆转了转移性癌细胞中染色质甲基化和乙酰化的变化。在3-D培养物中,抑制PGD即可阻断肿瘤形成。因此,研究者认为PGD可能是作为一种营养物质感应机制:通过不断降低6PG来迫使细胞消耗更多的葡萄糖。
随后细胞将利用葡萄糖消耗产生的过量代谢产物,对细胞内相应染色质区域中的组蛋白进行乙酰化或去甲基化以促进形成肿瘤,并引起肿瘤细胞转移生长中所出现的大规模表观遗传学改变。
方法总结:研究者依靠人工筛选数据来寻找代谢物水平和染色质变化之间的联系。在转移性胰腺癌中发生改变的大染色质结构域,可能会出现数百种不同的信号,而且由于细胞代谢途径不同,其代谢产物也会发生改变。例如,葡萄糖代谢途径可以有很多种,而且每种都会产生不同的中间体。而对于那些没有办法手动分析这些大型数据集的人来说,McDonald建议找到可能与被研究疾病相关的代谢物模式,然后与生物信息学家一起量身定制算法,以便反映当前的生物学特征。
再来看看一个比较前沿的领域——干细胞
二、干细胞稳定性
研究项目:甲硫氨酸是一种必需氨基酸,意味着它必须由膳食蛋白质提供。它可以形成S-腺苷甲硫氨酸(SAM),可促使DNA和组蛋白甲基化。杜克大学药理学家和癌症生物学家 Jason Locasale研究小组则通过研究甲硫氨酸代谢以了解细胞如何感知代谢变化,以及它们是否可以将这些信息传达给染色质。
研究结果:SIRT1(一种高度保守的哺乳动物酶)可调控小鼠胚胎干细胞甲硫氨酸代谢,也可以调控表观遗传标记来控制细胞分化。当研究人员在小鼠胚胎干细胞中删除或敲除SIRT1时,突变细胞中的甲硫氨酸含量很高,但SAM水平较低,因而许多组蛋白甲基化标记丢失,也导致细胞的多能性丧失。但其他SIRT1活动未受影响。
该小组认为干细胞丧失多能性,因为将甲硫氨酸转化成SAM的酶受SIRT1调控。Locasale说:“我们知道,SAM和乙酰-CoA通过酶与染色质相互作用来建立这些表观遗传修饰,但是它发生的程度以及如何发生的机制仍有待解决。”
方法总结:为了研究哪些氨基酸代谢途径受到SIRT1敲除的影响,Locasale的研究小组转向了高分辨质谱,这使得研究人员能够在不到一个小时的时间内测量数百种代谢物的浓度。然后,他们将一种算法应用到这些数据中,将实验中的代谢物与代谢物的标准化库进行比较,以推断营养物质如何从一种代谢途径流向另一种代谢途径。
他们将质谱分析中的数据以多种方式进行分析:测量在给定时间点与染色质反应的所有代谢物,确定所有对甲硫氨酸水平变化有反应的代谢物,并测量多少变异在代谢中促成了染色质的变化。“当我们对代谢物流量有详细的了解时,我们可以快速验证科学假设,并根据需要生成不同的可能性,”Locasale说。“十年前,这样的工作会花费更多的时间和精力。”
最后看个老牌项目——T细胞
三.T细胞活化
研究项目:有氧糖酵解(Warburg效应)通常被认为是T细胞活化后的代谢特征。通过此代谢途径,T细胞即便处于有氧的环境中,胞内的葡萄糖也会被转化为厌氧过程中的典型产物3-碳乳酸酯分子,并且可增强促炎细胞因子IFN-γ的表达。
虽然已有研究证明,有氧糖酵解被抑制后,可增加了另一种酶与IFN-γmRNA的3'非翻译区(3'UTR)结合,从而降低了该基因的翻译。但纪念斯隆凯特琳癌症中心的免疫学家李铭 (Ming Li )的研究小组却发现,即便删除了3'UTR,有氧糖酵解过程并没有被恢复,IFN-γ表达水平仍处于下调状态。显然,有氧糖酵解促进IFN-γ表达的背后机制还不是很明确。
研究成果:研究通过构建乳酸脱氢酶A(LDHA,有氧糖酵解的关键酶)缺陷的T细胞小鼠系发现,相比野生型T细胞,突变的T细胞所消耗的葡萄糖要低约70%,并表达较低水平的干扰素γ(IFNγ)。
为了寻找基因表达和糖代谢之间的另一种联系,研究小组通过染色质免疫沉淀(ChIP-Seq)发现,野生型和LDHA敲除细胞存在不同的组蛋白乙酰化(促进基因表达)和基因表达模式。LDHA敲除细胞中86%的下调基因(包括IFNγ)显示组蛋白乙酰化减少。而在LDHA驱动有氧糖酵解的能量产生过程中,会促使线粒体维持乙酰辅酶A高浓度,增强Ifng的组蛋白乙酰化和转录,促进IFN-γ表达。因而,LDHA可能成为自身炎症性疾病治疗靶点。
方法总结:文章在试图阐明代谢物在表观遗传效应中所起的作用时,寻找了DNA甲基化或组蛋白乙酰化等特定变化,然后寻找可能产生这些标记所需要成分的代谢途径。
通过这三个激动人心的研究进展,我们可以看出高通量表观遗传技术在不久的将来会有越来越广泛的应用。