平均来说,用典型的融合方法制备的杂交瘤,1%~3%的孔会分泌能够与抗原反应的抗体。一旦使用两个独立的筛选试验确定了阳性克隆,这些细胞应该立即进行亚克隆,分离出能够分泌抗体的单克隆杂交瘤细胞,同时扩增并冻存该原始阳性克隆。阳性克隆中通常含有不止一种稳定的杂交瘤细胞,因此,必须再进行克隆,以便得到只分泌一种抗体的单个克隆的杂交瘤细胞。在原始孔中可能存在着不分泌抗体的杂交瘤细胞和含不稳定染色体的杂交瘤细胞,这些细胞的生长能力可能比分泌抗体的杂交瘤细胞更强。单细胞克隆化是一个漫长(数星期到数月)而辛苦的过程。但是对分离能够产生高水平预期抗体的稳定杂交瘤细胞是必需的。有几种同等价值的亚克隆方法可供使用,包括有限稀释法和软琼脂克隆法。
有限稀释法是一种简单、易操作的技术。无论选择哪种方法,杂交瘤细胞都要经历至少两轮亚克隆,以减少两个细胞正好粘在一起形成克隆的可能性。这不仅为分离单克隆杂交瘤细胞提供了机会,也为选择具备最佳生长特性和分泌高水平抗体的杂交瘤细胞提供了机会。
培养低密度的杂交瘤细胞需要滋养细胞或条件培养基以提供生长所需的生长因子。如上所述,滋养细胞可用同系动物的脾细胞、胸腺细胞或巨噬细胞。原代培养的细胞是生长因子的极好来源,由于其在体外生存能力有限,不会污染长期培养的杂交瘤细胞。从未接触过目的抗原的动物组织中制备单细胞悬液。这些细胞的铺板密度为2*104个细胞/孔(与细胞融合时铺板的滋养层细胞密度相比,亚克隆过程要用更高的细胞密度),0.1ml/孔(96孔细胞培养板)。同样,滋养细胞层至少应该在使用前1天铺板,使产生的生长因子积累在培养上清中,同时也可用来验证原代培养的细胞没有污染。另外,许多商品化的生长因子补充剂(很多都含有IL-6)可以取代饲养细胞的使用。
按照下面的操作程序可以获得单个克隆的细胞。对杂交瘤细胞进行适当的稀释以使细胞能以三种浓度铺板:100个细胞/孔、10个细胞/孔和1个细胞/孔。初始克隆鉴定出的抗体分泌阳性孔,让细胞生长到近80%的汇合,然后轻轻地重悬,并进行活细胞计数。取5000个活细胞转入装有5ml含HT的DMEM完全培养基(亚克隆过程中最好不要改变培养基成分)的聚丙烯锥形管中,这样形成的细胞悬液浓度为1000个细胞/ml。利用这种细胞悬液,依次进行10倍稀释,便可分别得到浓度为100个细胞/ml和10个细胞/ml的细胞悬液。在两块已添加滋养细胞或补充成分(100ul/孔)的96孔细胞培养板的最上面一行(A行)加入100ul浓度为1000个细胞/ml的细胞悬液,使每孔含有100个有活力的杂交瘤细胞。这种密度的细胞,大约在10d内能生长到汇合。在每块细胞培养板的B行,加入100ul浓度为100个细胞/ml的细胞悬液,使每孔中含有10个有活力的杂交瘤细胞。在细胞培养板的其他几行(C-H行)加入100ul浓度为10个细胞/ml的细胞悬液,使每孔含有1个有活力的杂交瘤细胞。
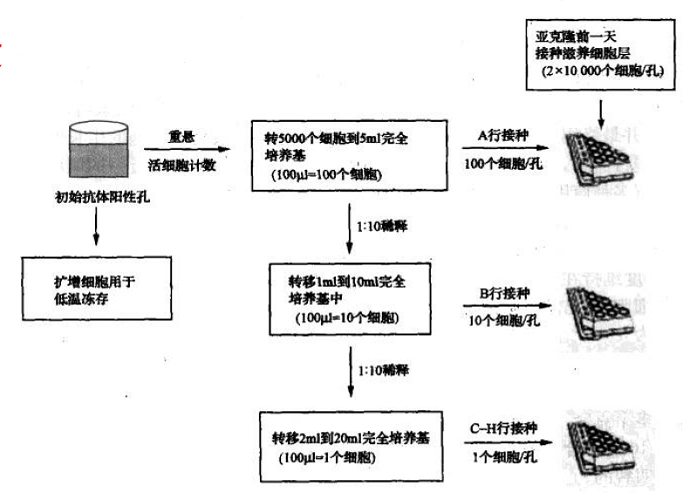
杂交瘤细胞的扩增和有限稀释法亚克隆程序
理想的结果是在每孔接种1个细胞的培养孔中能够收获到单克隆,然而,有时候阳性克隆很少或生长很慢,只能从接种较高密度接种的细胞孔中分离阳性克隆,因此,在一些孔中每孔接种10个细胞或100个细胞,当不能从接种单个细胞的孔中得到克隆时,可以从这些孔中得到。这种分离得到的不一定是单克隆,应该进行多轮亚克隆筛选。最好是从接种1个细胞的培养孔中选择克隆。
一旦单克隆的杂交瘤细胞系已确立并建库冻存,就应该换成不含HT的培养基培养细胞,并逐渐减少任何生长因子的添加。这可能需要多次传代的适应过程,每代减少一半的生长因子。这期间,细胞的增长率可能会降低;然而,这往往伴随着抗体产生的增加。在所有的添加物都已去除后,FBS的使用浓度也可减少。通常情况下,培养杂交瘤细胞的FBS浓度可以从20%、15%、12%,并最终过渡到10%。
细胞系在鉴定和分离的每一阶段都应该冻存:包括初始融合时鉴定的阳性克隆,第一轮和第二轮亚克隆的阳性克隆。此外,每一步应该冻存多个克隆,在关键的细胞系丢失后能从前面的冻存克隆中找回。一般来说,每次克隆冻存10管是合适的。液氮中的细胞可保持数十年。