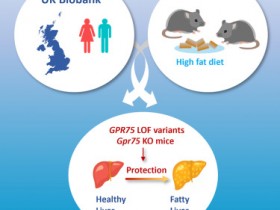
1、Cell:新方法绘制信息丰富的基因型-表型图谱
2022年6月9日,来自美国加州大学Jonathan S. Weissman和纪念斯隆凯特琳癌症中心Thomas M. Norman研究组合作在《细胞》上发表了标题为“Mapping information-rich genotype-phenotype landscapes with genome-scale Perturb-seq.”的研究成果,利用基因组尺度的Perturb-seq方法绘制了信息丰富的基因型-表型图谱。
据悉,遗传学的一个中心目标是揭示基因型和表型之间的关系。多表型筛选,例如Perturb-seq(具有单细胞RNA测序读数的基于CRISPR的筛选)可实现大规模筛选并行功能基因组作图,但迄今为止,其应用规模有限。
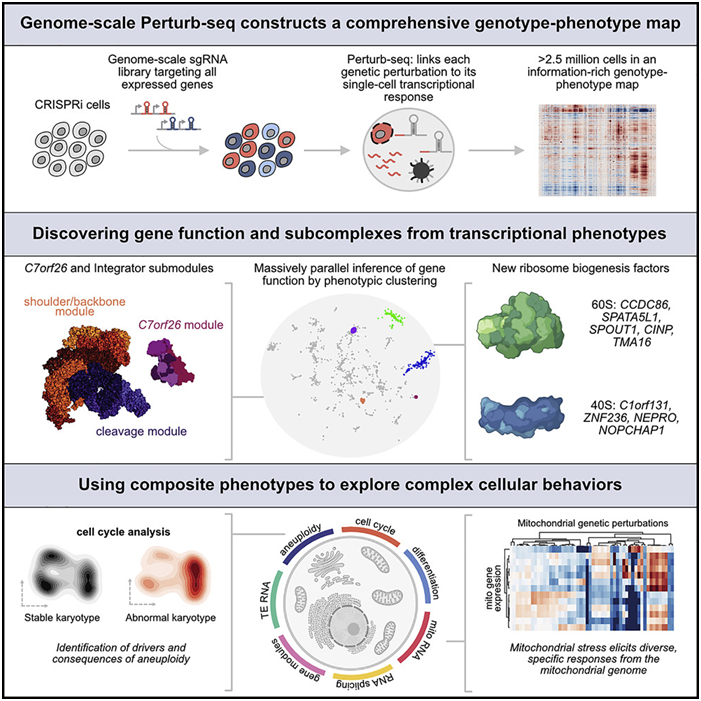
fig.1 | 图片来自cell
研究人员对超过250万个人类细胞进行了基因组规模Perturb-seq,针对所有表达的基因进行CRISPR干扰(CRISPRi)。研究使用转录表型来预测特征不明确基因的功能,揭示与核糖体生物发生(包括CCDC86、ZNF236和SPATA5L1)、转录(C7orf26)和线粒体呼吸(TMEM242)有关的新调节因子。除了确定基因功能外,单细胞转录表型还可以深入剖析复杂的细胞现象-从RNA加工到分化。
研究人员利用该方法系统地识别了非整倍性的遗传驱动因素和产生的后果,并意外发现了与线粒体基因组压力特异性调控有关的调控网络。该信息丰富的基因型-表型图揭示了基因和细胞功能的多维画像。
(评论:该图谱有利于人们能够深入研究各种生物学问题。用它来探索功能未知的基因对细胞的影响,研究线粒体对应激的反应,并筛选出导致染色体丢失或增加的基因,一种在过去被证明很难研究的表型。)
文章来源:
Joseph M. Replogle et al, Mapping information-rich genotype-phenotype landscapes with genome-scale Perturb-seq. DOI: 10.1016/j.cell.2022.05.013,Cell:最新IF:36.216
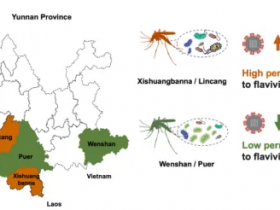
2、Nature:运动产生的Lac-Phe代谢物可抑制进食和肥胖
2022年6月15日,来自美国斯坦福大学医学院Jonathan Z. Long和贝勒医学院Yong Xu研究组合作在出版的《自然》杂志发表了标题为“An exercise-inducible metabolite that suppresses feeding and obesity. ”的研究新成果,发现运动产生的一种代谢物可抑制进食和肥胖。
运动可以预防肥胖型糖尿病和其他心脏代谢疾病。然而,运动产生有益于代谢的分子和细胞机制仍不清楚。
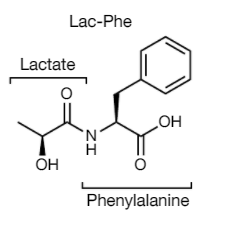
fig.2| 图片来自nature 截图
研究表明运动会刺激N-乳酰苯丙氨酸(Lac-Phe)的产生,这是一种抑制进食和肥胖的血源性信号代谢产物。通过乳酸和苯丙氨酸产生Lac-Phe的过程发生在CNDP2+细胞中,包括巨噬细胞、单核细胞和其他定位于不同器官的免疫细胞和上皮细胞。在饮食诱导的肥胖小鼠中,通过药物增加Lac-Phe的含量会减少食物摄入,而不会影响运动或能量消耗。长期服用Lac-Phe可降低肥胖和体重并改善葡萄糖稳态。相反,敲除小鼠体内与Lac-Phe生物合成相关基因会增加运动训练后的食物摄入和肥胖。
最后,在人类和赛马中也观察到运动会明显增加循环Lac-Phe的量,表明这种代谢物是与多种运动方式和哺乳动物身体活动相关的分子效应物。这些数据揭示了一种保守的运动诱导代谢物,它控制食物摄入并影响系统能量平衡。
(评论:这一研究标志着运动抑制食欲以及减轻体重过程的分子途径的起点,在运动对哺乳动物包括人体的影响上,有了更清晰的认知。意味着将来有可能利用Lac-Phe的分子水平,改善人们的体重管理。)
文章来源:
Li, Veronica L. et al,An exercise-inducible metabolite that suppresses feeding and obesity.DOI: 10.1038/s41586-022-04828-5,Nature:最新IF:43.07
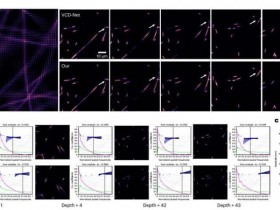
3、Nature:DNA双螺旋融化的机制
2022年6月15日,来自英国弗朗西斯·克里克研究所Alessandro Costa小组在《自然》杂志上发表了标题为“Mechanism of replication origin melting nucleated by CMG helicase assembly.”的研究成果,揭示DNA双螺旋融化的机制。
自从近70年前发现DNA的双螺旋结构以来,科学家们一直在努力了解两条DNA链是如何打开的,以访问它们所包含的遗传信息。这种开口对于包括DNA修复,基因表达和DNA复制用于细胞分裂的基本过程是必需的。
据研究人员介绍,真核生物复制起源的激活发生在时间上分离的步骤中,从而确保染色体在每个细胞周期只被复制一次。首先,MCM螺旋酶以非活性双六聚体的形式被加载到双联DNA上。激活发生在招募一组启动因子之后,这些因子组装了两个Cdc45-MCM-GINS(CMG)全螺旋酶。CMG的形成导致DNA在建立复制叉的过程中出现下绕,但DNA是否在这个阶段变得融化还不清楚。
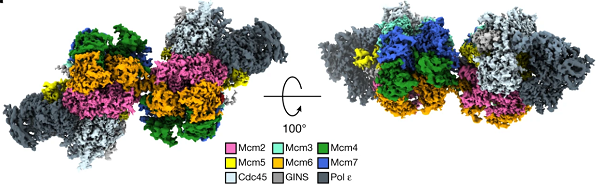
fig 3| dCMGE复合物 (图片来着nature截图)
通过用纯化的酵母蛋白在体外重新构建,研究人员用冷冻电镜观察了ATP依赖的CMG在染色质化源头上的组装。研究人员发现,CMG的形成破坏了双六聚体的界面,从而使两个CMG之间的双链DNA暴露。两个螺旋酶仍然被拴住,这就产生了一个伸展的二聚体,对源头激活和复制体的完整性有影响。在每个MCM环内,双螺旋变得不缠绕,碱基配对被破坏。这是ATP触发的MCM构象变化的结果,涉及DNA拉伸和蛋白质介导的三个孤儿碱基的稳定。在这个结构中,与DNA结合的Mcm2孔环残基对于双六聚体的装载和CMG的形成是可有可无的,但对于解除DNA的缠绕和促进复制是必不可少的。这些结果解释了ATP结合如何通过CMG使DNA成核并在起始阶段维持复制体的稳定性。
(评论:了解DNA双螺旋融化的机制为研究如何控制DNA复制的启动提供了基础。这对于理解染色体完整性的维持具有重要意义,这是一个在癌症中出错的过程。)
文章来源:
Lewis, Jacob S., Gross et al, Mechanism of replication origin melting nucleated by CMG helicase assembly.DOI: 10.1038/s41586-022-04829-4, Nature:最新IF:43.07