1、Cell:重大发现—大脑可存储和检索特定的免疫反应
2021年11月8日,来自以色列理工学院Asya Rolls研究组在《细胞》杂志发表了题为“Insular cortex neurons encode and retrieve specific immune responses.”的研究论文,发现岛叶皮层神经元编码和检索特定的免疫反应。
研究意义:越来越多的证据表明,大脑调节外周免疫力,但大脑是否以及如何代表免疫系统的状态仍不清楚。
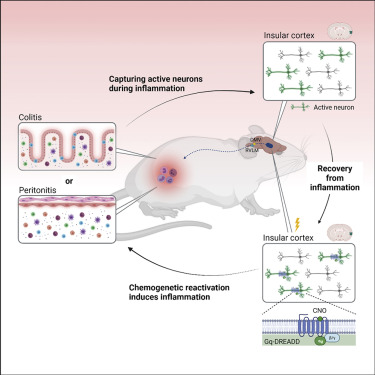
Fig1 |概图(来源:Cell截图)
研究人员表明大脑的岛叶皮层(InsCtx)储存着与免疫有关的信息。利用小鼠活动依赖性细胞标记(FosTRAP),研究人员捕获了InsCtx中在两种不同炎症条件下(葡聚糖硫酸钠[DSS]诱导的结肠炎和酵母聚糖诱导的腹膜炎)活跃的神经元集合。这些神经元组合的化学遗传重新激活足以广泛地检索这些神经元被捕获时的炎症状态。
因此,研究人员表明,大脑可以存储和检索特定的免疫反应,将免疫学记忆的经典概念扩展到炎症信息的神经元表征。
Highlights
- Neuronal ensembles in the InsCtx are activated during peripheral inflammation
- Reactivation of these neurons is sufficient to retrieve peripheral inflammation
- These InsCtx neurons project to autonomic nervous system control sites (DMV, RVLM)
- Inhibition of the InsCtx alleviates inflammation during DSS-induced colitis
(评论:机体的免疫反应不仅取决于免疫系统,还受到大脑和情绪的调节。这篇研究发现也为理解肠道炎症中的肠-脑轴机制,提供了新见解。)
文章来源:
Tamar Koren, Re’ee Yifa, Mariam Amer et al,Insular cortex neurons encode and retrieve specific immune responses. DOI: 10.1016/j.cell.2021.10.013, Cell:最新IF:36.216
2、Nature Genetics:生殖系致病性突变在肿瘤发生中的特定作用
2021年11月5日,来自美国纪念斯隆-凯特琳癌症中心Michael F. Berger团队在《自然—遗传学》发表了题为“The context-specific role of germline pathogenicity in tumorigenesis.”的研究成果,揭示种系致病性在肿瘤发生中的特定背景作用。
研究意义:人类癌症产生于环境、遗传和体细胞因素,但这些机制在肿瘤发生中是如何相互作用的,人们对此了解甚少。
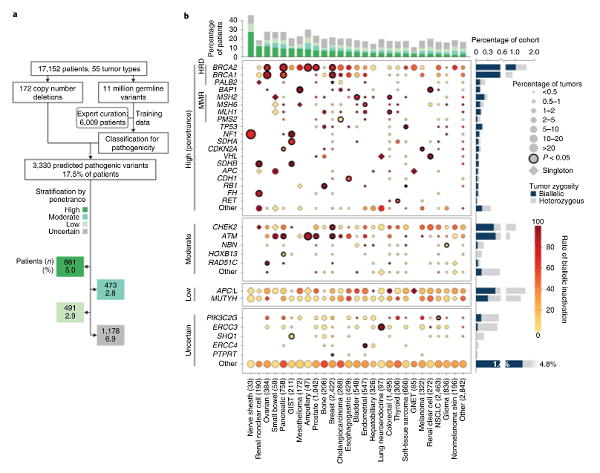
Fig 2 | 具有前瞻性特征的晚期癌症的种系致病性(来源:Nature Genetics截图)
通过研究17152名前瞻性测序的癌症患者,研究人员确定了癌症易感基因的致病种系变异,并评估了它们的合子型和伴随肿瘤的体细胞改变的共同发生。肿瘤发生的两个主要途径是明显的。在高致病性基因的致病性种系变体携带者中(总比例为5.1%),双亲失活的谱系依赖性模式导致肿瘤表现出机制特定的体细胞表型和较少的额外体细胞致癌驱动。
然而,这些患者中有27%的癌症,以及在低倾向性基因中具有致病性种系变异患者中的大多数肿瘤,缺乏与种系等位基因相关肿瘤发生的特殊特征。肿瘤对致病性种系变体的依赖性是可变的,而且往往由渗透率和血统决定,这一发现对临床管理有影响。
(评论:将外显率、体细胞双等位基因失活率、生殖系致病性突变、肿瘤类型等进行分层分析,发现体细胞突变和生殖系突变共同驱动肿瘤的发生和进展,并回答了以下几个问题: 为什么不同肿瘤的外显率会不一样; 为什么有些患者发病年龄很早 )
文章来源:
Srinivasan, Preethi, Bandlamudi et al, The context-specific role of germline pathogenicity in tumorigenesis. DOI: 10.1038/s41588-021-00949-1, Nature Genetics:最新IF:25.455
3、Nature:肠道共生菌群能够通过膳食氨基酸产生调节宿主免疫的脂质
2021年11月10日,来自美国哈佛医学院Dennis L. Kasper等研究人员合作在《自然》杂志上发表了题为“Host immunomodulatory lipids created by symbionts from dietary amino acids.”的研究成果,发现肠道共生菌群能够通过膳食氨基酸产生调节宿主免疫的脂质。
研究意义:来自共生微生物群的小分子对肠道免疫的成熟和调节起着至关重要的作用。然而,对于在宿主-微生物群环境中控制免疫发展的分子机制知之甚少。
研究人员使用靶向脂质组分析和合成方法,对来自人类共生体脆弱拟杆菌(Bacteroides fragilis)的免疫调节性α-半乳糖基神经酰胺(BfaGCs)进行了多方面的调查。BfaGCs的特征性末端支链是脆弱拟杆菌在宿主肠道中吸收支链氨基酸的结果。一个不能代谢支链氨基酸的脆弱拟杆菌基因敲除株显示BfaGCs的支链减少,并且只定植这种突变株的小鼠的自然杀伤T(NKT)细胞调节功能受损,这意味着结构特异的免疫调节活性。BfaGCs的鞘氨醇链支链是NKT细胞激活的一个关键决定因素,它能诱导特定的免疫调节基因表达特征和效应功能。CD1d-BfaGC-NKT细胞受体复合物的共结晶结构和亲和力分析证实了BfaGCs作为CD1d限制性配体的互动。
研究人员提出了一个通过内生代谢物与饮食、微生物群和免疫系统的相互作用实现免疫调节控制的新范式。
文章来源:
Oh, Sungwhan F., Praveena, T., Song et al, Host immunomodulatory lipids created by symbionts from dietary amino acids. DOI: 10.1038/s41586-021-04083-0, Nature:最新IF:43.07