2023年11月10日,来自美国加州大学Peter Tontonoz团队在《科学》杂志上发表了标题为”Aster-dependent nonvesicular transport facilitates dietary cholesterol uptake.“的研究成果,近期取得重要工作进展,研究发现Aster依赖性非囊泡型转运能促进膳食胆固醇摄取。
据介绍,肠道吸收是维持系统胆固醇稳态的重要因素。Niemann-Pick C1 Like 1(NPC1L1)有助于膳食胆固醇摄取的初始步骤,但胆固醇如何在NPC1L1下游移动尚不清楚。
研究人员发现Aster-B和Aster-C对肠细胞中的非囊泡型胆固醇转运至关重要。NPC1L1的缺失减少了可接近的质膜(PM)胆固醇,并消除了Aster向肠道边界的募集。缺乏Asters的肠细胞积累PM胆固醇,并显示内质网胆固醇耗竭。Aster缺乏的小鼠胆固醇吸收受损,可以预防饮食诱导的高胆固醇血症。最后,Aster通路可以用小分子抑制剂靶向,以控制胆固醇的摄取。
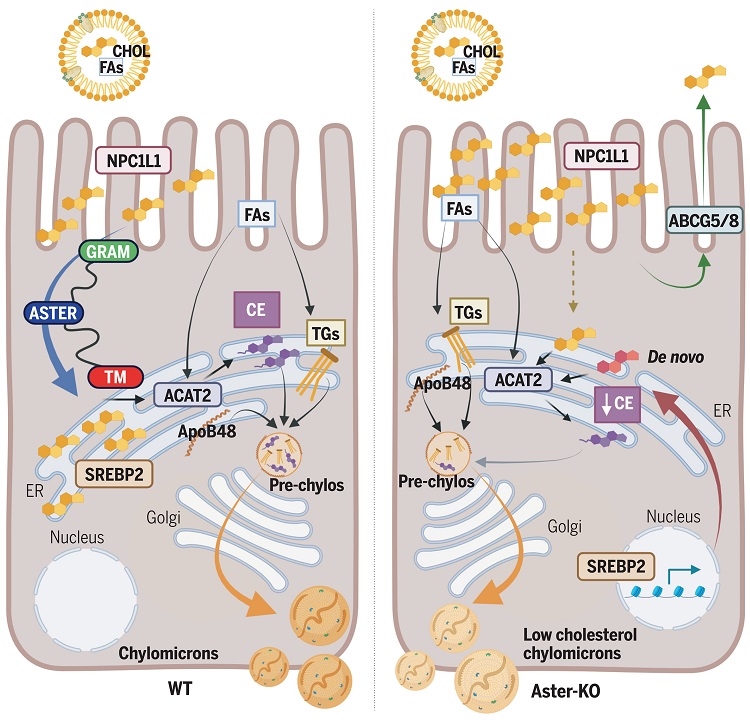
为了探究Aster蛋白在小肠胆固醇吸收中的功能,研究人员发现构建了Aster-B和-C双敲除(B/C-KO)的小鼠模型。研究人员发现发现,尽管NPC1L1的功能未受影响,但是B/C-KO小鼠对于食物中胆固醇的摄取能力大大降低。通过小肠类器官的体外培养实验,研究人员发现发现Aster缺失会引起胆固醇在小肠上皮细胞的细胞膜上累积,而内质网中胆固醇酯的水平则显著降低。另外,Aster缺失还会代偿性的激活内质网中SREBP2介导的胆固醇从头合成途径。因此,这些实验结果共同表明Aster缺失会破坏胆固醇从细胞膜向内质网的转运。进一步,作者发现Aster作用于NPC1L1的下游,具体而言,NPC1L1首先将细胞外的游离胆固醇转运至细胞膜中,当细胞膜上的胆固醇含量升高之后则会招募Aster到细胞膜并启动胆固醇从细胞膜向内质网的运输。
总之,该研究揭示由Aster蛋白介导的非囊泡转运途径是胆固醇由细胞膜进入内质网的主要途径。此外,他们的研究结果显示抑制Aster通路不仅可以降低小肠对于胆固醇的摄取,还可以预防高胆固醇饮食引起的高胆固醇血症。这些发现将Aster通路确定为膳食脂质吸收中一个生理上重要,且药理学上易于处理的节点。
文章来源:
Alessandra Ferrari, Emily Whang et al, Aster-dependent nonvesicular transport facilitates dietary cholesterol uptake.DOI: adf0966,Science,最新IF:63.714







