1、Science:肿瘤疫苗与CAR-T疗法的完美结合,可完全清除60%小鼠体内的实体瘤
近日,来自麻省理工学院达雷尔·欧文(Darrell Irvine)教授团队《Science》杂志上发表了题为“Enhanced CAR–T cell activity against solid tumors by vaccine boosting through the chimeric receptor”的研究。这项研究开创性地实现通过分子佐剂提升 CAR-T 细胞杀伤肿瘤细胞的效率,为研究者对抗实体瘤的攻坚战提供了新的思路。
该团队设计了一种癌症疫苗,最高能使注射进小鼠体内的CAR-T细胞数量提高200倍,多种抗肿瘤功能提升5-10倍。经该疫苗“涡轮增压”的CAR-T细胞大军,浩浩荡荡地杀向多种实体瘤,可以使60%模型小鼠的肿瘤完全消失。
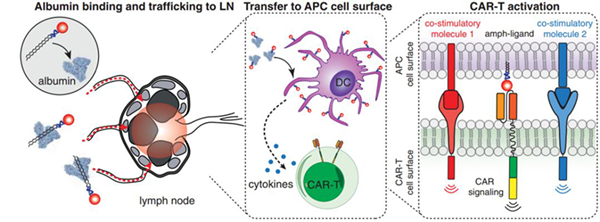
该团队利用白蛋白 (albumin) 在淋巴结中富集的性质,在分子佐剂中融合了可以结合白蛋白的结构域,使得包含有能调节免疫系统活性成分的分子佐剂能搭上白蛋白的“顺风车”进入淋巴结,发挥其免疫调控功能。
研究人员先给小鼠注射了5万个CAR-T细胞,随后又注射了两亲抗原和佐剂,一段时间后,发现CAR-T的比例最高达到了总T细胞的70%,在数量上是对照组的200倍。
研究人员在胶质母细胞瘤、乳腺和黑色素瘤等实体瘤小鼠模型中进行了检测,发现相比对照组,在两亲抗原的加持下,CAR-T细胞能够大幅缩小肿瘤的体积,延长肿瘤小鼠的生存期,并使得60%小鼠的实体肿瘤完全消失,并且没发现明显的毒副作用,效果好得惊人!
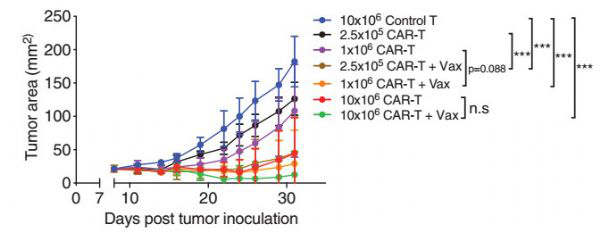
疫苗(Vax)大幅增强CAR-T抗癌效果
不仅如此,接受治疗的小鼠还保持了对癌细胞的长期免疫记忆,在开始治疗的75天后,再次注射同种癌细胞,这些癌细胞会很快被免疫系统清除。过了50天后,给这些小鼠注射少量其他种类的癌细胞,免疫系统竟然能将这些癌细胞也清除掉!
(评论:看来这种方法肯快就可以在患者身上进行测试了)
文章来源:
Ma L1,2, Dichwalkar T1, Chang JYH1, et al. Enhanced CAR-T cell activity against solid tumors by vaccine boosting through the chimeric receptor. Science. 2019 Jul 12;
2、Science: T细胞介导的微生物群调控可以防止肥胖
近日,来自近日,美国犹他大学健康学院的研究人员在《Science》杂志上发表了题为“T cell–mediated regulation of the microbiota protects against obesity.”的研究结果,表明肠道中有一种特定的梭状芽孢杆菌(Clostridia)可以防止小鼠变胖,这些细菌同样也可以控制人类的体重。这一发现可能会给治疗肥胖带来新的方法,这些方法比恢复微生物群落的粪便移植或基于益生菌的策略更有优势。
研究人员将目光集中于一种基因工程免疫缺陷小鼠(T细胞已禁用Myd88信号传导),这种小鼠在肠道中表现出缺陷的T滤泡辅助细胞(TFH细胞)发育和IgA生成。缺乏肠道IgA的产生意味着,动物无法有效控制肠道微生物组的组成。研究小组发现,这些免疫缺陷小鼠随着年龄的增长,会不可避免地变得肥胖,即使喂食正常的“食物”,它们也会患上许多肥胖人类身上发现的与肥胖相关的代谢疾病。
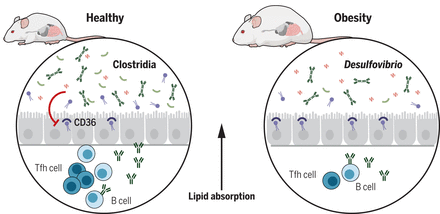
图 来源Science
不可避免地变得肥胖的小鼠,其免疫系统受损,肠道菌群中一种叫做梭状芽胞杆菌的细菌比健康小鼠少。给免疫受损的小鼠注射梭状芽胞杆菌可以预防肥胖。
对比基因工程免疫缺陷小鼠和正常小鼠,进一步研究发现,免疫缺陷小鼠的肠道微生物群落中多种梭状芽孢杆菌的数量和多样性均有减少,另一种名为脱硫弧菌(Desulfovibrio)的细菌数量却明显增加了。而这种弧菌与炎症性肠病、2型糖尿病和肥胖症有关。当研究人员向免疫缺陷小鼠体内补充梭状芽孢杆菌时,动物的体重增加要少的多。这表明,梭状芽孢杆菌的缺失与免疫缺陷小鼠的肥胖有因果关系。
(评论: 这项工作将开启新的研究——关于免疫反应如何调节微生物群和代谢疾病)
文章来源:
Petersen C el al. T cell–mediated regulation of the microbiota protects against obesity. Science (2019).
3、Science:IFITM蛋白抑制胎盘合胞滋养细胞的形成,促进胎儿死亡
近日,来自法国巴斯德研究所等研究人员在《Science》杂志上发表了题为“TIFITM proteins inhibit placental syncytiotrophoblast formation and promote fetal demise.”的研究结果,确定了一种改变胎盘发育的新机制,可能在怀孕期间引起严重的并发症。这种新机制与干扰素的产生有关。
胎盘既是交换的界面,也是母亲和胎儿之间的屏障。它提供胎儿生长所需的营养,并产生激素,保护胎儿免受微生物和母体免疫系统的侵害。胎盘的外层,称为合体滋养细胞(syncytiotrophoblast),它是由外层细胞融合而成,优化胎盘的屏障和交换功能。
细胞融合是由一种称为合胞素(syncytin)的蛋白质介导的。如果合体滋养细胞不能正确形成,那么可能导致胎盘功能不全并影响胎儿发育。对于胎儿宫内发育缓慢或胎儿患有唐氏综合症的女性,医生往往观察到异常的合体滋养细胞。
干扰素(interferon)是在感染期间由免疫细胞产生的物质,用来对抗病毒和其他细胞内微生物。在自身免疫疾病或炎性疾病(比如狼疮)以及一些病毒感染中,研究人员观察到高水平的干扰素。
(评论:对IFITM功能的鉴定让我们更好地了解与胎盘发育相关的机制,以及在感染或其他疾病过程中它如何被破坏。)
文章来源:
Buchrieser J, Degrelle SA, Couderc T, et al. IFITM proteins inhibit placental syncytiotrophoblast formation and promote fetal demise. Science. 2019 Jul 12;








