蛋白质的纯度和质量对下游实验应用非常重要,糟糕的样品通常会导致许多的问题,造成实验的不准确和低精确性,有时甚至还会导致实验完全失败。本文主要回顾在使用不好的蛋白质样本会遇到的问题,以及如何分析目的蛋白的纯度和完整性。有许多可用的技术,可以相互配合使用,以提供最准确全面的蛋白质样品状态图。
一、导致蛋白质样品质量差的问题
- 不当的控制有时会导致蛋白质发生错误折叠、聚集或从溶液析出,这通常是一个不可逆的过程(如盐析)。聚集和降解也会影响蛋白质的天然状态,使其无法正确地与其他蛋白质或分子结合。有时候,肉眼也可以清楚地看到样本的聚集情况。
- 当酶失活或错误折叠时,会导致酶分析实验失败或复现性很差。如果使用酶分析作为目的蛋白的指示,这是特别重要的。
- 蛋白质的水解除了有丢失精心构建的功能标签的风险外,也会导致上述问题。虽然有一些试剂可以减少蛋白质样品的水解和降解,但当蛋白质储存在水溶液中时,总是存在水解的风险。
显然,投入一些时间仔细控制影响蛋白质质量的因素是很重要的,如对储存条件做一些控制,包括pH值、缓冲液、盐浓度、蛋白质浓度和储存温度等。即使在最优的制备和储存条件下,蛋白质的质量也会随着时间而变化,所以应该定期检查蛋白质样品,以确保它们符合实验要求。在开始使用耗时或昂贵的技术之前,花点时间检查下蛋白质的质量是值得的,从长远来看,有助于节省时间和金钱。
二、测定蛋白质纯度和质量的可靠方法
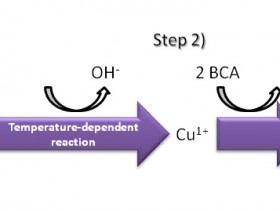
- 一般定量:UV-Vis、Bradford法和活性测定
通常,我们需要测量蛋白质样品的浓度。紫外可见分光光度法和Bradford法是高通量的,几乎在每个生物化学实验室都使用,相对酶活性测定更粗糙些。UV-Vis和Bradford法的检测结果取决于样本中的总蛋白质,不仅仅是目的蛋白。而活性测定具有目标特异性,测量纯化样品中活性蛋白含量,但并不是所有的蛋白质都可以用活性分析来定量。
Abbkine为您精心推荐蛋白质定量组合方案:蛋白质定量优选方案:BCA法和Bradford法
| 产品名称 | 货号 |
| Protein Quantification Kit (BCA Assay) | KTD3001 |
| Protein Quantification Kit (Bradford Assay) | KTD3002 |
- 粒径分析:电泳
和上面描述的定量方法一样,电泳也是被生物化学家广泛使用,它可以提供目标蛋白的大小以及是否存在其他蛋白质杂质的一般情况。在进行电泳之前,需要对你的蛋白质浓度有一个大概的了解。
电泳方法有几种,最常见的是变性SDS-PAGE。样品首先用SDS(一种洗涤剂)变性,然后利用电场在聚丙烯酰胺凝胶基质上按质量分离。在非变形PAGE中,蛋白质的分离更为复杂,它是根据非变性结构的净电荷、大小和形状进行的。这两种技术都可以识别出样品中是否存在“弥散”带样的降解,如果凝胶中蛋白质含量过高,也会发生这种情况。
但电泳不能显示低水平的杂质或微小的尺寸差异,电泳也需要0.1 ~ 2mg /mL浓度的样品来提供清晰的结果。
- 粒径分析:质谱分析法
质谱分析是一种非常强大的分析技术,它可以非常准确和精确地识别翻译后的修饰,而用上述技术是不容易可视化的。电离质谱法的工作原理是通过质量和电荷分离蛋白质或多肽,将它们加速到检测器上,并为每种蛋白质(或蛋白质片段)创建一个独特的光谱。
单纯依靠质谱法评价蛋白质质量的缺点是其相对低通量,需要大量的样品制备。此外,很难评估样品中的蛋白质是否完整,因为这一过程是变性的,不能识别错误折叠。
- 均匀性:动态光散射
如果目的蛋白质用上述方法看起来是纯的,可以继续检查下它是否分散在样品中而不是发生聚集。动态光散射(DLS)使用偏振光测量样品中含有小分子(或蛋白质)的衍射水平。当样品通过仪器时,发生的散射量是溶液中粒子流体动力半径的影响。
虽然DLS是一种易于使用的技术,它提供了优秀的定性信息,但它不能提供蛋白质样品中粒径分布的全面图像,因为聚合体很容易压倒检测器。这种方法也不适用于评估四级结构(二聚体与单体)。DLS的便利性和它随时间推移显示聚集形成的能力使其成为一种广泛使用的评估均匀性的方法。
- 微流体扩散分级(MDS)(流体分析)
微流体扩散分级(MDS)是一种快速、简便的蛋白质粒径和浓度测定方法,是衡量蛋白质质量的重要指标。MDS使用微流控分析芯片将蛋白质样本送入一个通道,在这个通道中,蛋白质样本与辅助流体一起以稳定的层流状态流动,没有混合。蛋白质从一个流转移到另一个的唯一途径是扩散,扩散的速率与蛋白质的大小(流体动力学半径,Rh)成正比。经过一定的扩散后,这两种流再次分离,蛋白质被标记。用扩散比和未扩散比计算Rh。
MDS避免了其他技术的一些缺陷,蛋白质和基质之间没有相互作用,就像在电泳中一样,样品是在其自然状态下运行的。所需的工作流程很简单,10分钟之内得到结果,样品浓度低至约10µg/mL。