可能很多人都听过白介素这个词,但是他们到底是啥大伙还不清楚,先简单科普下:
人类研究炎症反应的历史十分悠久。最初人们发现白细胞可以产生一些调控自身功能的细胞因子。这些细胞因子对于炎症反应的发生发展都有着调控作用,根据其产生的来源,将其命名为白细胞介素,简称白介素。白介素的发现,使得人们对于炎症反应的认识更加深入,原来,机体可以通过分泌不同的白介素来调动相应的免疫细胞大军发挥不同的功能,比如我们熟知的感染引发的红肿发热反应就是有很多不同白介素介导的。随后,人们发现不只是白细胞,很多细胞都可以分泌白介素,而白介素的功能也不仅仅是局限在对于白细胞的功能调控,很多细胞都可以对白介素做出反应。虽然现在仍然在沿用白介素这一统称,但白介素其实是一组由多种类型细胞所分泌的、结构和功能各异的可溶性蛋白,这些分泌出来的蛋白主要用于不同细胞间的信息交换。
白介素种类很多且功能各异,但有个被称为白介素-17家族很引人瞩目,他们对炎症反应的发生发展起着不可忽视的作用,该家族的细胞因子被分别命名为白介素-17A到白介素-17F。同时,人们还找到了它们的受体家族:白介素-17受体A到白介素-17受体E。这些白介素-17细胞因子可以结合到相对应的受体成员上从而介导不同的炎症反应。白介素-17的发现为以前一些有争议的炎症现象提供了合理的解释,同时也使得人们对于炎症信号网络的认识更加细致深入。科学家从小鼠的T细胞淋巴瘤细胞中首先发现了白介素-17A,通过生物信息学手段,很快发现在基因组中还含有其他五个和白介素-17A同源的基因,由此,人们将这六个同源的细胞因子归入一个新的白介素家族:白介素-17家族。
该家族中最具代表性的成员当然是老大哥白介素-17A了,在机体受感染或损伤处,迁移过来的淋巴细胞会分泌白介素-17A。白介素-17A一方面会诱导炎症因子以及趋化因子的表达,从而招募更多的免疫细胞到达炎症部位加剧机体的炎症反应,另一方面,白介素-17A还会诱导一些组织修复相关因子的表达从而加速机体的恢复。虽然白介素-17A在宿主抗感染和组织修复过程中起到扩大免疫防御反应保护自身机体的作用,但是,在很多自身免疫病病人和肿瘤病人当中,白介素-17A又是高表达的,由于它可以诱导很多炎症因子的表达,过高的白介素-17A水平对于疾病的病理发展起到恶化作用。很多动物实验也证明,白介素-17A缺失或者抗体中和白介素-17A,可以有效的抑制多种自身免疫病病理程度。因此,白介素-17家族的细胞因子就如同一把双刃剑,在急性炎症反应中,它们可以快速的分泌出来保护机体不受外源有害物质的危害,而当人体产生由于多种遗传和环境因素所导致的慢性炎症时,它们又会加速多种慢性疾病的病程。所以,白介素-17家族细胞因子和人类的健康息息相关。

最近人们对白介素-17A这个明星细胞因子又有了新的认识:动物学以及人类流行病学分析显示,如果母亲在怀孕期间感染某些病毒,那么她的后代患自闭症或者神经发育紊乱的风险就会增加。过去的研究表明,这种在怀孕期间由母体引发的免疫反应学术上称之为母体免疫激活(MIA,maternal immune activation),该反应会导致后代出现一些不正常的重复行为,而导致该现象发生的部分原因可能是因为白介素-17A(由多种发炎条件下一组辅助T细胞——Th17细胞——产生)在其中起作用。然而,这类现象背后更深层次的分子细胞生物学机制至今仍然研究的不是很清楚。来自美国麻省大学医学院的Jun R. huh(已move到哈佛医学院)和MIT的Gloria B. Choi合作,在过去研究的基础之上进一步研究表明了孕妇肠道细菌能在怀孕期间刺激Th17细胞的产生,从而意味着其后代更有可能出现MIA相关的行为异常。该工作以“Maternal gut bacteria promote neurodevelopmental abnormalities in mouse offspring”为题在线发表在9月13日的Nature杂志上。
上述研究首先证明了白介素-17A只可能在怀孕的母鼠中分泌然后导致MIA相关的行为异常出现。进一步研究发现,如果母鼠在怀孕期间受感染的话,带有小鼠分节丝状菌(segmented filamentous bacteria)或人体共生菌(它们能诱导肠道Th17细胞)的怀孕小鼠可能会增加其后代患神经发育障碍的风险,而如果通过穿刺技术用特异性的抗生素处理孕鼠,那么就不会出现MIA相关的后代行为异常。
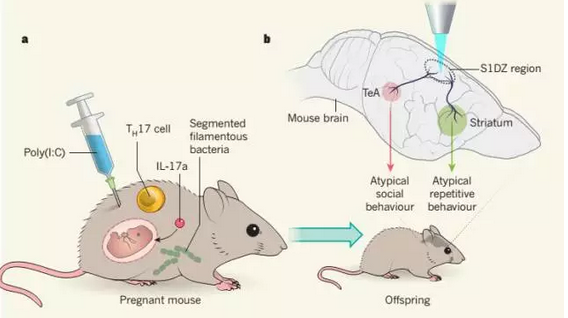
而在另一篇同样由Gloria B. Choi和Jun R. huh合作完成的题为“Reversing behavioural abnormalities in mice exposed to maternal inflammation”的Nature长文论文中(事实上两篇Nature是同时投稿和被接受的),研究人员找出了小鼠大脑中引发行为异常的区域——大脑异颗粒区初级躯体感觉皮质部位(dysgranular zone of the primary somatosensory cortex, S1DZ),随后他们又通过光遗传学的手段进一步发现S1DZ区域的激活就可以导致小鼠出现与病毒感染类似的MIA相关的后代行为异常;反之,如果抑制S1DZ区域的激活,那么即便是母鼠出现MIA也不会导致后代行为异常。
值得一提的是,针对上述两项研究成果,来自美国德克萨斯西南医学中心的Craig M. Powell 还专门为此撰写了题为“Mum’s bacteria linked to baby’s behaviour”的评论文章。Craig Powell在评论中尖锐的指出孕期感染相关病毒与后代出现自闭症性状关联性仍然不清楚,同时Craig Powell还提到,如果上述关联着实存在,那么在孕期调节孕妇肠道的有关菌群不失为降低后代发生自闭症性状风险的一种可行的手段。有意思的是,Craig Powell还写道,即便上述两篇论文描述的机制不存在于人类自闭症中,那么这些论文揭示的肠道细菌、免疫系统和大脑发育之间的复杂相互作用,仍然为科学家提供了有价值的新见解。
相关产品推荐:








