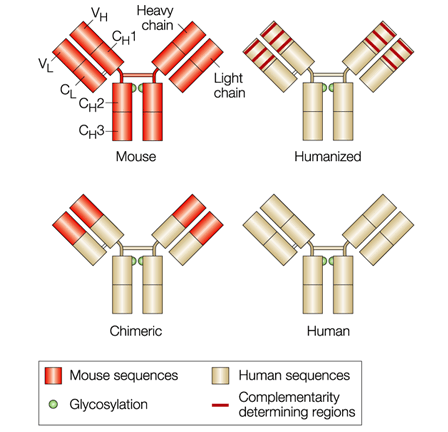
随着基因工程技术的迅速发展,治疗性单抗经历了从100% 的鼠源单抗 (Mab),到嵌合抗体,人源化抗体(Humanized Mab),到全人源性抗体的过程,逐步消除了异源性抗体的免疫原性问题,在保持对抗原高亲和力的同时,改善了抗体的药代动力学。
单抗药物主要是由中国仓鼠卵巢细胞(Chinese hamster ovary cell,简称 CHO 细胞) 表达产生,由 CHO 细胞分泌的外源蛋白分子,通过纯化过程实现由细胞培养液中回收。根据终产品纯度、杂质含量的严格要求,单抗目前采用三步纯化策略:粗纯 (样品捕获)、中度纯化和精细纯化。目前,约70-80% 的抗体纯化使用 Protein A、 Protein G 亲和层析,一步纯化可使蛋白纯度达 95%以上。
在生物药物的生产过程中,为避免细菌、内毒素或病毒的污染, 需要对层析系统、 介质等进行在位清洗 (CIP),NaOH是最好的除菌、除热源的试剂。同时NaOH也是公认的CIP试剂,使用NaOH可以很好的除去残留在层析介质上的杂质,以确保工艺的稳定性以及层析介质的寿命,而且NaoH的成本低。天然或重组的蛋白 A 配基对 NaOH非常敏感,强碱性条件下易变性或脱落,因此只能选用高浓度的盐酸胍或尿素进行清洗,但清洗的效果远远不如NaOH,而且清洗成本非常高。
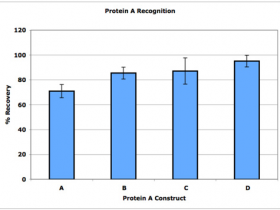
PurKine™ Protein AT Resin的配体蛋白 Protein At 是在天然蛋白 A 的基础上进行生物工程突变得到的一种耐碱蛋白 A (Alkaline tolerate, At), 去除了不耐受NaOH的氨基酸,提高了层析介质耐受NaOH的能力。 PurKine™ Protein AT Resin 4FF以高度交联的4%琼脂糖凝胶为基质,可以在相对较高的流速进行单克隆抗体和多克隆抗体的纯化,该产品以 0.1M NaOH 进行 200 次在位清洗,介质载量几乎不变,以 0.5M NaOH 进行 100 次在位清洗,载量仍可达到最初载量的 80%。该产品采用较稳定的定向偶联,配基脱落量低(小于 10ng/mg IgG),宿主蛋白(HCP)和宿主DNA(HCD)的残留量低,非常适用于工业化抗体的大规模生产。
pH、盐浓度、 buffer 种类、温度等都会影响抗体的聚集动力学。 如 pH<3,抗体会发生不可逆聚集; 没有保护剂的情况下IgG浓度高于 2mg/ml 容易形成二、多聚体等。除上面提到的各种杂质外,治疗用抗体在生产和纯化过程中还会由于糖基化程度不同、蛋白酶作用、以及脱氨基和脱酰胺等反应而产生带电性质不同的多种抗体变体。由于蛋白A层析介质对聚体没有去除作用,在蛋白A捕获步骤中主要去除的杂质大部分是HCP和基因组DNA。
所以必须注意,特别是CHO细胞表达基因工程抗体 (Gab)的过程中,由于细胞培养过程带来的糖基化的不均一以及后期的脱氨基脱酰胺等作用,存在着等电点不同的多种抗体变体,建议在中度纯化和精细纯化阶段,用阳离子交换层析捕获浓缩抗体或流穿模式的阴离子交换层析,根据带电性质的不同有效去除这些变体,使产品性质更均一。