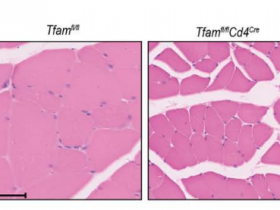
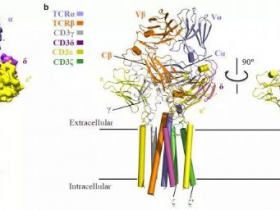
2024年1月11日,来自美国加州大学Jennifer A. Doudna团队在《自然—生物技术》杂志上发表了标题为"In vivo human T cell engineering with enveloped delivery vehicles."的研究成果,研究开发了人体内T细胞工程包膜运载工具。
据介绍,病毒和病毒来源的颗粒具有向细胞递送分子的内在能力,但很难轻易改变细胞类型的选择性,这阻碍了它们用于治疗递送。
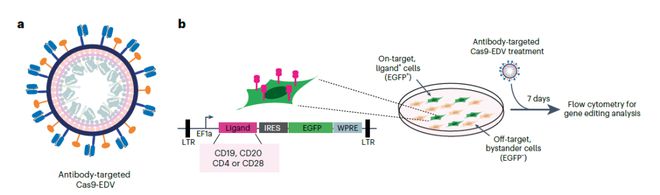
Cas9-EDV的设计原理和在细胞培养情况下的验证实验
研究人员表明,通过显示在封装CRISPR–Cas9蛋白和引导RNA的膜来源颗粒上的抗体片段识别细胞表面标记物,可以将基因组编辑工具传递到特定细胞。与依赖进化的衣壳趋向性来传递病毒编码货物的腺相关病毒等传统载体相比,这些Cas9包装包膜递送载体(Cas9-EDV)利用可预测的抗体-抗原相互作用,将基因组编辑器选择性地瞬时递送到感兴趣的细胞。在混合群体中,抗体靶向的Cas9 EDV优先在同源靶细胞中进行基因组编辑。
总之,通过使用多重靶向分子直接递送到人T 细胞,Cas9 EDV能够人源化小鼠中产生基因组编辑的嵌合抗原受体T细胞,建立了一种具有广泛治疗应用潜力的可编程递送模式。
文章来源:
Hamilton, Jennifer R., Chen, Evelyn, Perez, Barbara S. et al, In vivo human T cell engineering with enveloped delivery vehicles.Nature Biotechnology:最新IF:68.164