总结
PARP 1和PARP 2在DNA损伤反应(DDR)中通过感知DNA中的单个断裂并通过组蛋白和其他蛋白质的多聚ADP核糖基化来募集修复机制而起作用。PARP抑制剂对与PARP途径互补的修复途径缺陷的癌细胞具有细胞毒性,并且已经显示这些抑制剂中的一些通过将PARP 1/2捕获到DNA上而起作用,从而阻止修复并导致细胞死亡。因此,DNA捕获是PARP抑制剂的高度期望的性质。
为了支持具有捕获能力的新型PARP抑制剂的发现,我们开发了一种创新的PARPtrap™测定法,该测定法设计用于小分子文库的高通量筛选,并特异性鉴定或比较能够将PARP 1和/或PARP 2捕获到DNA上的抑制剂(1)。
介绍
DNA损伤,导致碱基错配、大体积加合物、交联、单链断裂或双链断裂,由多种外源性和内源性机制发生。为了保持基因组的完整性,以应对DNA损伤,哺乳动物细胞采用一系列的修复机制。启动的DNA修复途径取决于损伤的类型,并且高度依赖于环境。修复途径还可以触发细胞周期阻滞、应激反应和凋亡。
聚ADP核糖聚合酶(PARP)是一个由17个成员组成的蛋白质大家族,它们是DDR的关键启动子(2)。在PARP家族中,PARP 1至3特异性地参与损伤感知、损伤位点处的修复蛋白的募集和激活、基因组维持和细胞死亡。PARP1和PARP2主要参与DNA修复,两种蛋白质都调节DDR网络。PARP2还调节表观遗传、增殖和炎症过程,对精原细胞、胸腺和脂肪组织发育非常重要(3,4)。相比之下,PARP1改变转录,并诱导细胞凋亡时,DNA损伤无法修复,因此可能发挥更突出的作用作为一个治疗靶点。
由于保持基因组完整性对生物体至关重要,至少有150种不同的蛋白质形成了复杂的DDR网络,不断扫描和修复DNA。事实上,在缺乏适当修复的情况下,基因组不稳定性导致遗传变化的积累,这些变化可能直接导致肿瘤的形成。例如,BRCA1(乳腺癌1型易感蛋白1)和BRCA2突变损害细胞通过同源重组(HR)修复双链DNA断裂的能力,增加了人对乳腺癌,卵巢癌或前列腺癌的易感性(3)。然而,HR依赖性DNA修复的丧失意味着这些肿瘤细胞依赖于其他修复途径生存,暴露了治疗的弱点。
科学家们在合成致死性的背景下利用了这一点,合成致死性是由两种蛋白质同时破坏引起的细胞死亡,而当每种蛋白质单独受损时,没有活力丧失。因此,HR缺陷本身不会杀死细胞,但添加PARP抑制剂可通过特异性阻断互补DNA修复途径有效靶向HR缺陷癌细胞进行凋亡(6)。
目前有四种PARP 1/2抑制剂在美国获批用于临床,另外两种在中国获批,还有许多其他药物正在进入临床(前)阶段。

表1:目前临床上使用的PARP抑制剂。
批准的抑制剂的新临床应用仍在扩大,因为现在已经确定,阻断肿瘤细胞中的任何HR途径(不限于BRCA基因)都会赋予“BRCA”,并且在PARP抑制剂存在下对细胞是致命的。事实上,PARP抑制剂还抑制DNA修复,以响应诱导单链DNA断裂的放射性或化学疗法,为这种治疗类别以不同的治疗组合治疗各种肿瘤铺平了道路
发现DNA捕获作为PARP抑制剂的作用机制
在第一种PARP抑制剂进入临床开发大约十年后,人们发现除了阻断PARP 1的酶活性外,PARP抑制剂还可以将PARP锁定在DNA上
什么是DNA陷阱?
作为第一反应者,PARP 1和PARP 2感知DNA中的单链断裂,并在将聚ADP核糖(PAR)链添加到其自身的蛋白质骨架、组蛋白和其他修复蛋白之前立即与其结合,以便招募和激活它们。由于PAR链的强静电荷,PAR化的PARP然后从DNA分离,允许其他蛋白质启动修复过程。通过PARG(Poly(ADP-ribose)glycohydrolase,聚腺苷二磷酸核糖)糖水解酶)去除PAR链,使PARP恢复其失活形式,并准备再次检测DNA损伤。
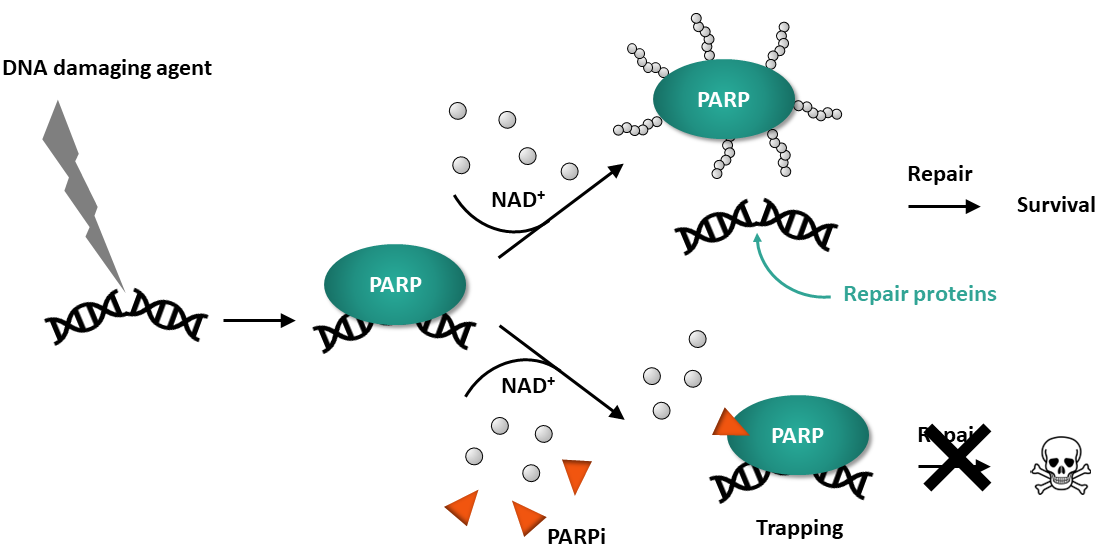
图1:PARP与DNA单链断裂结合并被激活。自动PAR化降低了其对DNA的亲和力,导致解离。一种阻止DNA释放的PARP抑制剂被称为“陷阱”PARP到DNA上。
目前批准的药物通过与NAD+结合竞争并阻止自动PAR化来降低PARP1和PARP2的活性,导致无法从DNA上分离。PARP在损伤部位的持续存在阻止修复并阻断复制,导致细胞死亡。因此,将PARP捕获到DNA的药物往往比捕获能力弱的PARP抑制剂具有更大的细胞毒性(9)。
在抑制PARP 1/2的四种临床药物中,三种在捕获PARP 1和PARP 2的效力上不同,而不考虑其抑制PARP催化活性的效力(4,8,9)。事实上,这类药物的细胞毒性作用及其临床疗效似乎与它们如何有效地将PARP蛋白捕获到受损的DNA上,作为细胞毒素(10)。
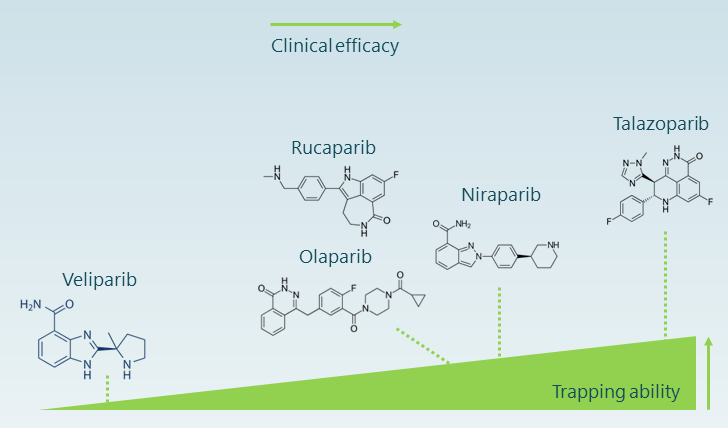
图2:PARP抑制剂与其已知捕获DNA能力相关的临床疗效增加。
此外,科学家最近观察到,将PARP1捕获到DNA而不是PARP2,会导致细胞毒性增加。因此,此类抑制剂的筛选应包括定量PARP捕获能力并区分抑制剂对PARP 1或PARP 2的选择性的测定(3,8)。
PARPtrap™测定专门评估药物将PARP捕获到DNA上的能力。
大多数市售PARP测定法测量其酶活性并定量靶蛋白(如组蛋白)的PAR化。相反,PARPtrap™测定测量化合物将PARP 1或PARP 2保持在DNA探针上的能力,而不是测量其对PARP酶活性的影响。
这种均相、简单的检测方法可以用于高通量药物发现筛选或优化增强捕获的分子。PARPtrap™分析使研究人员能够有效地筛选他们的文库中最有效的抑制剂。
该测定基于荧光偏振原理,并使用荧光标记的DNA探针,当被偏振光激发时,其发射具有与分子旋转速率成比例的偏振度的荧光。游离DNA探针非常小且旋转快速,因此它们具有低荧光偏振(FP)。当与PARP复合时,由于蛋白质尺寸较大,分子旋转缓慢,并且荧光偏振度较高。加入NAD+后,新的PAR化酶与探针分离,降低FP水平(见图3)。
在实践中,用户将纯化的PARP1或PARP2与特异性荧光DNA探针一起孵育,然后添加NAD+以启动PAR化。一旦PAR化,由于PAR链的高负电荷,PARP与探针分离。这是FP最低的实验条件,因为大多数DNA探针将是游离的。
用阻断PAR化但不阻断与DNA结合的抑制剂预孵育PARP将使酶保持被捕获到DNA探针上,在这种情况下,探针保持与PARP形成复合物,导致高FP。因此,用户比较低FP下的无抑制剂对照和高FP下的测试抑制剂条件,这意味着FP信号的增加指示抑制剂的捕获。

图3:PARPtrap™测定的原理。
有关荧光偏振原理的更详细综述以及FP检测的使用和分析提示,请访问我们的常见问题解答和技术说明。请记住,该测定需要能够阅读荧光偏振的荧光酶标仪(能够发射偏振光并测量水平和垂直窗格之间的荧光差异)。
已知抑制剂捕获PARP1和PARP2的效力的比较
两种测定,对应于PARP1和PARP2,探针特异性和酶动力学进行了优化,显示出相似的范围和灵敏度。每种检测均使用经酶法验证的纯化PARP 1或PARP 2蛋白。
在图4所示的实验中,分别使用PARP1的PARPtrap™测定试剂盒(#80584)和PARP2的PARPtrap ™测定试剂盒(#78296),在浓度增加的Talazoparib、奥拉帕尼、Veliparib和AZD 5305存在下测量PARP1捕获(左)和PARP2捕获(右)。“无化合物”对应于测定法允许的最低FP,“无NAD+”对应于测定法允许的最高FP。如通过EC50所测量的,在两个图上指示每种药物的功效。
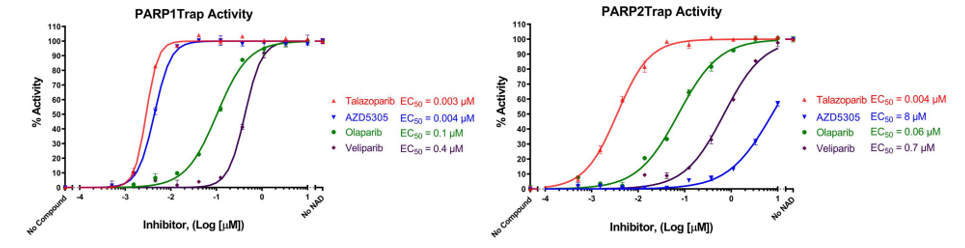
图4:PARP抑制剂对PARP 1和PARP 2的捕获。在浓度增加的Talazoparib、Olaparib、Veliparib和AZD 5305存在下测量的DNA上的PARP捕获(#78318)使用PARPtrap™测定试剂盒,BPS Bioscience,#80584𓇘.“无化合物”对应于“低FP对照”,“无NAD”对应于“高FP对照”。
Talazoparib、Olaparib和Veliparib对PARP1和PARP2具有相似的捕获功效,如通过其EC50测量的,而AZD 5305在捕获PARP1方面比PARP2有效1,000倍,证明了PARP1和PARP2之间的选择性。在试验中观察到的Talazoparib、Olaparib和Veliparib的相对捕获效力与已知的相对临床效力相似(8)。在这些试验中,AZD 5305对PARP1的DNA捕获活性与Talazoparib一样有效。
这些结果表明,通过定量PARP捕获能力,该试验可以区分抑制剂对PARP 1或PARP 2的选择性,从而提供关于哪种抑制剂可能证明更具细胞毒性的线索。
| 产品名称 | 货号 | 规格 |
| PARP 抑制剂套装 | 78318 | 8x50ul |
| PARPtrap™ Assay Kit for PARP2 | 78296-1 78296-2 |
96 reactions 384 reactions |
| PARPtrap™ 组合检测试剂盒(适用于PARP1 和PARP2) | 78317 | 384rxns |
| PARPtrap™ Assay Kit for PARP1 | 80584 | 96 reactions 384 reactions |
结论
BPS Bioscience开发了一种均匀,简单的检测方法,可用于高通量药物发现筛选,以增强DNA上PARP1或PARP2的捕获。因此,PARPtrap™是一种独特的检测方法,使科学家能够有效地筛选他们的文库中最具特异性和有效的抑制剂。此外,用于PARP1和PARP2的PARPtrap™ Combo Assay Kit(#78317)在相同测定中比较分子捕获PARP1与PARP2的能力,从而允许直接比较化合物对每种PARP同工酶的效力。
优势
- 简单的程序
- 从开始到结束仅需3小时
- 免洗
- 检测化合物对PARP 1和PARP 2的效力差异
- 96-孔或384孔
References
(1) Zientara-Rytter K, et al. 2023 Cancer Research 83(7_Supplement): 6111.
(2) Ummarino S, et al. 2021 Genes 12(3): 446.
(3) Ali SO, et al. 2016 Am. J. Cancer Res. 6(9): 1842-1863.
(4) Rose M, et al. 2020 Front. Cell Dev. Biol. 8: 564601.
(5) Wood RD, et al. 2001 Science 291: 1284-1289.
(6) Rudolph J, et al. 2022 PNAS USA, 119(11): e2121979119.
(7) Lord CJ, Ashworth A. 2016 Nat. Rev. Cancer 16(2): 110-120.
(8) Murai J, et al. 2012 Cancer Res. 72: 5588–99.
(9) Krastev DB, et al. 2021 Cancer Res. 81(22): 5605-5607.
(10) Pommier Y, et al. 2016 Sci. Transl. Med. 8(368): 368er7.







